题目内容
9.某工厂使用石油热裂解的副产物CH4来制取H2,其生产流程如图1所示: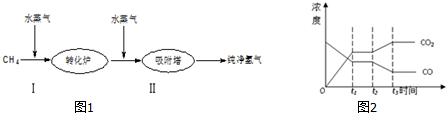
(1)第II步反应为CO(g)+H2O(g)?H2(g)+CO2(g)△H<0,其平衡常数随温度的变化如下:
| 温度T/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(2)第II步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,向恒容反应器中加入下列物质发生上述反应,其中反应开始时,向正反应方向进行的有B(填实验编号).
| 实验编号 | n(CO)/mol | n(H2O)/mol | n(H2)/mol | n(CO2)/mol |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
①体系的压强不再变化 ②混合气体的平均相对分子质量不再变化
③体系中各物质的浓度不再改变 ④体系的温度不再变化
⑤混合气体的密度不再变化
(4)图2表示此流程的第II步反应在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况.则图中t2时刻发生改变的条件是降低温度或增加水蒸汽的量或减少氢气的量(只写2种).
(5)若400℃时,第Ⅱ步反应生成l molH2放出的热量为 33.2kJ,第Ⅰ步反应的热化学方程式为 CH4(g)+H2O(g)═CO(g)+3H2(g)△H=-103.3kJ•mol-1.
则400℃时,CH4和水蒸气反应生成CO2和H2的热化学方程式为CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=-136.5kJ•mol-1.
分析 (1)依据化学平衡三段式列式计算,设一氧化碳消耗物质的量为x,
830℃,CO(g)+H2O(g)?H2(g)+CO2(g),
开始 1 1 0 0
转化 x x x x
平衡 1-x 1-x x x
利用830℃下K计算CO的转化率;
(2)利用Q与K的关系可知,Q<K时反应向正反应反应移动;
(3)利用平衡的特征“定”、“等”及由此衍生的物理量来分析;
(4)t2时二氧化碳的浓度增大,而CO的浓度减小,该反应正向移动,以此分析;
(5)①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-33.2kJ•mol-1,
②CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3kJ•mol-1,
由盖斯定律可知,①+②得到CH4(g)+2H2O(g)=4H2(g)+CO2(g).
解答 解:(1)设一氧化碳消耗物质的量为x,
830℃,CO(g)+H2O(g)?H2(g)+CO2(g),
开始 1 1 0 0
转化 x x x x
平衡 1-x 1-x x x
K=$\frac{x×x}{(1-x)(1-x)}$=1,解得x=0.5,
则CO的转化率为$\frac{0.5mol}{1mol}$×100%=50%,
故答案为:50%;
(2)A.Q=$\frac{2×3}{1×5}$=1.2>K=1,则向你反应方向移动,故A不选;
B.Q=$\frac{1×1}{2×2}$=0.25<K=1,则反应向正反应反应移动,故B选;
C.Q=$\frac{1×1}{0.5×2}$=K,平衡不移动,故C不选;
故答案为:B;
(3)①该反应的压强始终不变,则体系的压强不再发生变化,不能判断平衡,故①不选;
②混合气体的总质量、总物质的量始终不变,则混合气体的平均相对分子质量不变,不能判断平衡,故②不选;
③各组分的物质的量浓度不再改变,为平衡的特征,能判断平衡,故③选;
④体系的温度不再发生变化,反应达到平衡,故④选;
⑤固定容积,质量、体积始终不变,则混合气体的密度不变,不能判断平衡,故⑤不选;
故答案为:③④;
(4)t2时二氧化碳的浓度增大,而CO的浓度减小,该反应正向移动,则改变的条件为降低温度或增加水蒸汽的量或减少氢气的量,
故答案为:降低温度或增加水蒸汽的量或减少氢气的量;
(5)①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-33.2kJ•mol-1,
②CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3kJ•mol-1,
由盖斯定律可知,①+②得到CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5kJ•mol-1,
故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=-136.5kJ•mol-1.
点评 本题考查较综合,涉及化学平衡的计算、平衡的判定、热化学反应方程式等,注重高考常考查点的考查,注意习题中的数据和图象的分析,题目难度中等.

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案| A. | 一定温度和压强下,将 0.5mo1N2和 1.5mo1H2 置于密闭容器中充分反应生成 NH3(g),放 热 19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |||||||||
| B. | H2 标准燃烧热△H=-285.8 kJ•mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |||||||||
| C. | C(石墨)═C(金刚石)△H=+1.9kJ•mol-1,说明石墨比金刚石稳定 | |||||||||
| D. | 通常人们把拆开 1 mol 某化学键所吸收的能量看成该化学键的键能:
|
| A. | 1molNa2O2晶体中阴离子的个数为2NA | |
| B. | 1 mol•Lˉ1FeCl3溶液含有的Cl-数为3 NA | |
| C. | 标准状况下,2.24L苯所含的分子数为0.1NA | |
| D. | 32g O2和32g O3 所含的氧原子数都是为2NA |