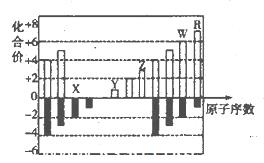
题目内容
(每空2分,共12分)下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格: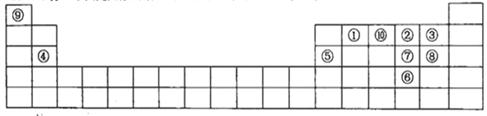
(1)在这10种元素中,非金属性最强的是___________(填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为______________________,元素②与⑨形成的18e-化合物的电子式____________________;
(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有___________________________;
(4)比较元素⑦⑧形成的气态氢化物的稳定性:____>____(用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式______________________。
(1)③ ;H-O-Cl;(2)H—O—Cl ; 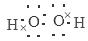 ;
;
(3)离子键和共价键; (4)HCl>H2S ; (5)Al2O3+2OH- = 2AlO2- +H2O
解析试题分析:(1)根据元素在周期表中的位置可知:在这10种元素中,非金属性最强的是③F元素;(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为H-O-Cl;元素②与⑨形成的18e-化合物H2O2的电子式是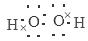 ,(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M:NH4NO3中含有的化学键类型有离子键、极性共价键;(4)由于非金属性Cl>S,所以元素⑦⑧形成的气态氢化物的稳定性:HCl>H2S ;(5)元素⑤Al的氧化物与氢氧化钠溶液反应的离子方程式是l2O3+2OH- = 2AlO2- +H2O。
,(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M:NH4NO3中含有的化学键类型有离子键、极性共价键;(4)由于非金属性Cl>S,所以元素⑦⑧形成的气态氢化物的稳定性:HCl>H2S ;(5)元素⑤Al的氧化物与氢氧化钠溶液反应的离子方程式是l2O3+2OH- = 2AlO2- +H2O。
考点:考查元素的推断、元素周期律的应用、元素形成的化合物的结构、性质及化学用语的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列说法中正确的是
| A.第三周期所包含的元素中钠的原子半径最小 |
| B.钠的第一电离能比镁的第一电离能大 |
| C.在所有元素中,氟的电负性最大 |
| D.电子云示意图中的每个小黑点都表示一个电子 |
下列排列顺序正确的是( )
① 热稳定性:H2O>HF>H2S ② 原子半径:Na>Mg>O
③ 酸性:H3PO4>H2SO4>HClO4 ④ 熔沸点:H2O>HF>HCl
| A.①③ | B.②④ | C.①④ | D.②③ |
(10分)A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
| A | | C |
| | B | |
(1)A、B、C三种元素的名称分别为 、 、 。
(2)B位于元素周期表中第 周期、第 族。
(3)C的原子结构示意图为 ,C的单质与
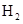 反应的化学方
反应的化学方 程式为 。
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式 。