题目内容
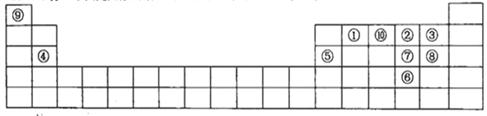
下列排列顺序正确的是( )
① 热稳定性:H2O>HF>H2S ② 原子半径:Na>Mg>O
③ 酸性:H3PO4>H2SO4>HClO4 ④ 熔沸点:H2O>HF>HCl
| A.①③ | B.②④ | C.①④ | D.②③ |
B
解析试题分析:非金属性越强,氢化物的稳定性越强,①不正确,热稳定性应该是HF>H2O>H2S;同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则选项②正确;非金属性越强,最高价氧化物的水化物的酸性越强,③不正确,酸性应该是HClO4>H2SO4>H3PO4;水、HF分子间均存在氢键,熔沸点偏高,选项④正确,答案选B。
考点:考查元素周期律的应用
点评:该题主要是考查学生对元素周期律的熟悉了解程度,以及灵活运用元素周期律解决实际问题的能力,难度不大。该题的关键是熟练记住元素周期律的具体内容,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力和灵活应变能力。

练习册系列答案
相关题目
下列关于元素周期表的说法中,不正确的是( )
| A.周期表的16族中,第ⅢB族所含的元素种类数最多 |
| B.在周期表中,元素的族序数都等于其原子的最外层电子数 |
| C.副族元素和第Ⅷ族元素都属于过渡金属 |
| D.第ⅦA族的砹(At),其单质为有色固体,AgAt不溶于水 |
下列叙述中能说明金属A肯定比金属B的活泼性强的是 ( )
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子电子层数比B原子电子层数多 |
| C.1mol A从酸中置换出的H2比1molB从酸中置换的H2多 |
| D.常温时,A能从稀盐酸中置换出氢,而B不能 |
下列排列顺序不正确的是
| A.热稳定性:CH4> SiH4 >HF | B.原子半径:Na>Mg>O |
| C.酸性:HClO4>H2SO4>H3PO4 | D.非金属性:F>Cl>Br |
1907年2月2日,享誉世界的俄国化学家门捷列夫因心肌梗塞与世长辞,那一天距离他的73岁生日只有六天。门捷列夫在科学界的主要贡献是
| A.发现色盲现象 | B.发现元素周期律 |
| C.发明硝酸甘油炸药 | D.发现了放射性元素钋 |
下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| D.Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |