题目内容
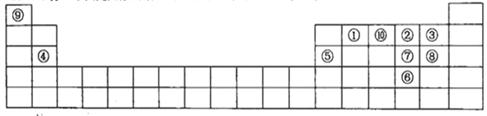
(10分)A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
| A | | C |
| | B | |
(1)A、B、C三种元素的名称分别为 、 、 。
(2)B位于元素周期表中第 周期、第 族。
(3)C的原子结构示意图为 ,C的单质与
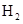 反应的化学方
反应的化学方 程式为 。
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式 。
(1)氮、硫、氟 (2)三 ⅥA
(3)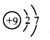 ;F2+H2="2HF"
;F2+H2="2HF"
(4)2NH3+H2SO4═(NH4)2SO4
解析试题分析:(1)依题意,A、B、C为短周期元素,从A、B、C的相对位置看,A、C只能处在第二周期,而B处在第三周期.设A的原子序数为x-1,则C为x+1,B为x+8,则有:(x-1)+x+1=x+8 x=8.所以A、B、C的原子序数分别为7、16、9,对应的元素分别为N、S、F,故答案为:氮 硫 氟。
(2)S位于第三周期ⅥA主族。
(3)F原子核外有2个电子层,最外层7个电子,原子结构示意图为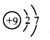 ;F2与H2反应生成氟化氢,化学方程式为:F2+H2=2HF
;F2与H2反应生成氟化氢,化学方程式为:F2+H2=2HF
(4)A的气态氢化物NH3与B的最高价氧化物对应水化物H2SO4反应生成(NH4)2SO4,化学方程式为:2NH3+H2SO4═(NH4)2SO4
考点:本题考查元素的推断、原子结构、元素周期表、结构示意图和方程式的书写。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
下列说法正确的是( )
| A.IA族元素的金属性比IIA族元素的金属性强 |
| B.VIA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
下列排列顺序不正确的是
| A.热稳定性:CH4> SiH4 >HF | B.原子半径:Na>Mg>O |
| C.酸性:HClO4>H2SO4>H3PO4 | D.非金属性:F>Cl>Br |
下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| D.Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
(8分每空1分)
(1)下列3种不同粒子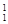 H、
H、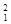 H、
H、 H表示______种元素,______种核素,
H表示______种元素,______种核素,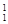 H、
H、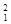 H、
H、 H互称为__________________。
H互称为__________________。
(2)下列各组物质中,互称为同分异构体的是( )
| A.水与冰 | B.O2与O3 |
C.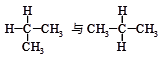 | D. |
(3)K2O: ;(4)CO2: 。
下表是元素周期表的一部分,针对所给的元素,完成下列各小题。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | | | | C | N | O | |
| 3 | Na | | Al | Si | | S | Cl |
21. 第3周期中金属性最强的元素是 (填元素名称)。
22. C、N和O原子半径由小到大的顺序的是 。
23. 第3周期中气态氢化物最稳定的是 (填化学式)。
24. Si是带来人类文明的重要元素之一,其氧化物化学式是 。
25. 铝是大自然赐予人类的宝物。它的一个用途是发生铝热反应,冶炼某些难熔金属,写出
该反应的一个化学方程式 。
26. S元素形成的氢化物与其氧化物SO2相遇后的现象是 。
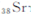 )元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与
)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与
 同属于第ⅡA族?
同属于第ⅡA族?