题目内容
(10分)下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):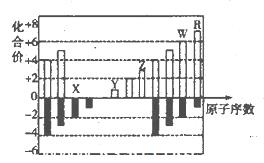
(1)元素x、Y、z、W、R五种元素中属于金属元素的是___________;Z的简单离子的结构示意图是___________。
(2)由此图可以判断,11种元素中处于同主族的共有____________组。
(3)X、Y.Z三种元素的原子半径大小顺序为___________;它们的离子的半径大小顺序为____________。
(1)Na、Al; ;
;
(2)4
(3)Na>Al>O;O2->Na+>Al3+
解析试题分析:(1)从化合价及原子序数上判断,X是O元素,Y是Na元素,Z是Al元素,W是S元素,R是Cl元素,所以这5种元素中属于金属元素的是Na、Al;Al3+的原子核内有13个质子,核外有10个电子,离子结构示意图为 ;
;
(2)依据同主族元素的化合价规律判断,最高正价与负价分别完全相同的元素属于同主族,但O常见- 2价,与S同主族;F无正价,与Cl同主族,所以共有4组属于同主族的元素;
(3)O、Na、Al的原子半径的比较依据电子层数越多,原子半径越大,核电荷数越少原子半径越大,三者的原子半径的大小顺序是Na>Al>O;三者的离子结构相同,所以离子半径的大小依据核电荷数越少,离子半径越大,所以离子半径的大小顺序是O2->Na+>Al3+
考点:考查元素周期律中的化合价规律,判断元素的类别,半径的比较

练习册系列答案
相关题目
下表是元素周期表的一部分,针对所给的元素,完成下列各小题。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | | | | C | N | O | |
| 3 | Na | | Al | Si | | S | Cl |
21. 第3周期中金属性最强的元素是 (填元素名称)。
22. C、N和O原子半径由小到大的顺序的是 。
23. 第3周期中气态氢化物最稳定的是 (填化学式)。
24. Si是带来人类文明的重要元素之一,其氧化物化学式是 。
25. 铝是大自然赐予人类的宝物。它的一个用途是发生铝热反应,冶炼某些难熔金属,写出
该反应的一个化学方程式 。
26. S元素形成的氢化物与其氧化物SO2相遇后的现象是 。
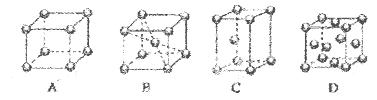
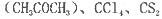 等互溶。
等互溶。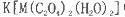 中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。
中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。