题目内容
4.下列有关金属及其化合物的说法正确的是( )| A. | 铜粉与稀硫酸不反应,但加入一定量硝酸钠后铜粉会发生溶解 | |
| B. | 金属Na久置于空气中最终产物是生成Na2O2 | |
| C. | Mg比Al活泼,更易与NaOH溶液反应生成H2 | |
| D. | 水蒸气通过灼热的铁粉有红棕色固体生成 |
分析 A.硝酸根离子在酸性条件下具有强氧化性;
B.Na2O2不稳定;
C.镁与氢氧化钠溶液不反应;
D.高温下,水与铁反应生成四氧化三铁.
解答 解:A.硝酸根离子在酸性条件下具有强氧化性,可氧化铜生成铜离子,故A正确;
B.Na2O2不稳定,应最终生成碳酸钠,故B错误;
C.镁与氢氧化钠溶液不反应,铝可与氢氧化钠溶液反应生成氢气,故C错误;
D.高温下,水与铁反应生成四氧化三铁,为黑色晶体,故D错误.
故选A.
点评 本题综合考查常见金属的性质与应用,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意把握物质的性质,难道不大.

练习册系列答案
相关题目
15.下列能表示化学反应速率的单位的是( )
| A. | mol/L | B. | mol/S | C. | mol/L•S | D. | mol/(L•min) |
12.下列物质属于纯净物的是( )
| A. | 液氯 | B. | 漂白粉 | C. | 新制氯水 | D. | 水玻璃 |
19.元素周期表中短周期的一部分如右图,关于X、Y、Z、W、Q说法正确的是( )


| A. | 元素Y与元素Z的最高正化合价之和的数值等于9 | |
| B. | 原子半径的大小顺序为:W>Z>Y | |
| C. | 离子半径的大小顺序为:W2->Y2->Z3+ | |
| D. | W的气态氢化物的热稳定性和还原性均比Q的氢化物的强 |
9.结合如图装置判断,下列叙述正确的是( )


| A. | 若X为NaCl,K与M相连时,石墨电极反应为:2Cl--2e-═Cl2↑ | |
| B. | 若X为NaCI,K与N相连时,溶液中有Fe2+生成 | |
| C. | 若X为稀硫酸,K与N相连时,溶液中H+向Fe电极移动 | |
| D. | 若X为稀硫酸,K与M相连时,Fe作负极受到保护 |
16.下列叙述正确的是( )
| A. | 分子式为C3H6有机物最多存在4个C-C单键,与C5H12的碳碳单键数相同 | |
| B. | 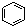 和 和  均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 | |
| C. | 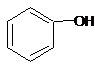 和 和 分子组成相差一个-CH2-,因此是同系物 分子组成相差一个-CH2-,因此是同系物 | |
| D. | 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此推测可能有H-O键 |
13.下列难溶盐的饱和溶液中,Ag+浓度最大的是( )
| A. | AgCl(Ksp=1.56×10-10) | B. | Ag2CO3(Ksp=8.1×10-12) | ||
| C. | Ag2CrO4(Ksp=9.0×10-12) | D. | AgBr(Ksp=5.0×10-13) |
14.下列反应的离子反应方程式书写正确的是( )
| A. | 向碘化钾溶液中加入用硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| B. | 向碳酸氢铵溶液中加入过量的稀氢氧化钠溶液:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| C. | 向Ba(OH)2溶液中加入过量NH4HSO4:Ba2++H++NH4++2OH-+SO 42-═BaSO4↓+H2O+NH3•H2O | |
| D. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+═2Fe3++3H2O |