题目内容
19.元素周期表中短周期的一部分如右图,关于X、Y、Z、W、Q说法正确的是( )
| A. | 元素Y与元素Z的最高正化合价之和的数值等于9 | |
| B. | 原子半径的大小顺序为:W>Z>Y | |
| C. | 离子半径的大小顺序为:W2->Y2->Z3+ | |
| D. | W的气态氢化物的热稳定性和还原性均比Q的氢化物的强 |
分析 由元素在周期表中的位置可知,X为N元素,Y为O元素,W为S元素,Z为Al,Q为Cl.
A.氧元素没有最高正化+6;
B.同周期自左而右原子半径减小、同主族自上而下原子半径增大;
C.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多,离子半径越大;
D.非金属性越强,氢化物的稳定性越强、氢化物还原性越弱.
解答 解:由元素在周期表中的位置可知,X为N元素,Y为O元素,W为S元素,Z为Al,Q为Cl.
A.Al元素最高正化合价为+3,氧元素没有最高正化+6,二者最高正化合价不是9,故A错误;
B.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径:Z>W>Y,故B错误;
C.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多,离子半径越大,故离子半径:S2->O2->Al3+,故C正确;
D.非金属性Cl>S,非金属性越强,氢化物的稳定性越强、氢化物还原性越弱,故D错误,
故选C.
点评 本题考查元素周期表与元素周期律,难度不大,注意对元素周期律的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列有关化学用语使用不正确的是( )
| A. | 原子核内有l8个中子的氯原子:${\;}_{17}^{35}$Cl | |
| B. | S2-的结构示意图: | |
| C. | CO2分子比例模型: | |
| D. | H2O2的电子式: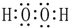 |
4.下列有关金属及其化合物的说法正确的是( )
| A. | 铜粉与稀硫酸不反应,但加入一定量硝酸钠后铜粉会发生溶解 | |
| B. | 金属Na久置于空气中最终产物是生成Na2O2 | |
| C. | Mg比Al活泼,更易与NaOH溶液反应生成H2 | |
| D. | 水蒸气通过灼热的铁粉有红棕色固体生成 |
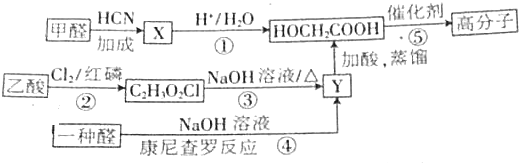
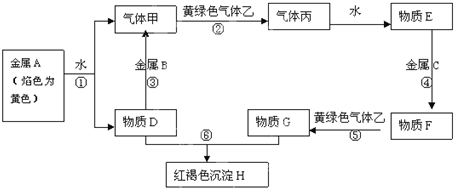
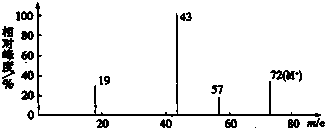
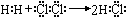 ;
;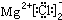 ,
,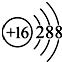
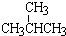 和
和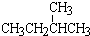 ; ②
; ②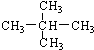 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).