��Ŀ����
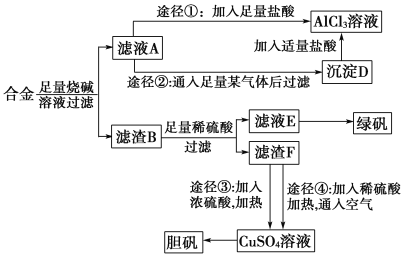
����Ŀ��ij��ѧ��ȤС����ֻ������������ͭ�Ĺ�ҵ�Ͻ���ȡ�������Ȼ�����Һ���̷�����(FeSO4��7H2O)�͵������壬��ʵ�鷽����ͼ��ʾ��
(1)�Ͻ���NaOH��Һ��Ӧ�����ӷ���ʽΪ_________________________________________��
(2)������;���ڵ����ӷ���ʽ________________________________________________��
D�м���������������ӷ���ʽΪ________________________________________________��
(3)����F����Ҫ�ɷ�Ϊ____________________
(4)CuSO4��Һ�л�õ����IJ���Ϊ����Ũ����_____________������_��ϴ�ӡ���Ȼ���
���𰸡�2Al��2OH����2H2O=2AlO2-��3H2�� AlO2-��CO2��2H2O=Al(OH)3����HCO3- Al(OH)3��3H��=Al3����3H2O Cu��ͭ���� ��ȴ�ᾧ
��������
������������ͭ�Ĺ�ҵ�Ͻ���������ռ���Һ����˵õ���ҺA������B����ҺAΪƫ��������Һ��ͨ��;���ټ����������ᷴӦ�����Ȼ��ơ��Ȼ��ƺ�ˮ��ͨ��;����ͨ������ij�������˵õ�����D����ij����Ϊ������̼������DΪAl(OH)3������BΪͭ�����Ļ�����������ϡ�������˵õ���ҺEΪ����������Һ�����Ʊ��̷����õ�����FΪͭ��ͭͨ��;���ۼ���Ũ���ᣬ�����Ƶ�����ͭ��Һ����ͨ��;���ܼ���ϡ������Ȳ�ͨ�����Ҳ���Ƶ�����ͭ��Һ������ͭ��Һͨ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ��������ݴ˷�����
(1)�Ͻ�����������ͭ�Ĺ�ҵ�Ͻ�ֻ��������NaOH��Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al��2OH����2H2O=2AlO2-��3H2����
(2)������;����ͨ������ij�������˵õ�����D����ij����Ϊ������̼������DΪAl(OH)3����Ӧ�����ӷ���ʽΪAlO2-��CO2��2H2O=Al(OH)3����HCO3-��
D�м����������ᷴӦ�����Ȼ�����ˮ����Ӧ�����ӷ���ʽΪAl(OH)3��3H��=Al3����3H2O��
(3)����F����Ҫ�ɷ�ΪCu��ͭ���ʣ�
(4)CuSO4��Һ�л�õ����IJ���Ϊ����Ũ������ȴ�ᾧ�����ˣ�ϴ�ӡ���Ȼ���