题目内容
20.在下列溶液中,各组离子一定能够大量共存的是( )| A. | 滴入甲基橙试液显红色的溶液:Mg2+、Al3+、Br-、SO42- | |
| B. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液中:Na+、NH4+、ClO-、I- | |
| C. | 0.1mol/LNaHCO3溶液中:K+、Ba2+、OH-、Cl- | |
| D. | 加入铝粉放出大量H2的溶液中:Fe2+、K+、Cl-、NO3- |
分析 A.滴入甲基橙试液显红色的溶液中存在大量的氢离子,四种离子之间不发生反应,都不与氢离子反应;
B.常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液为酸性溶液,次氯酸根离子能够氧化碘离子,次氯酸根离子能够与氢离子反应生成次氯酸;
C.氢氧根离子与碳酸氢钠反应生成碳酸钠;
D.加入铝粉放出大量H2的溶液为酸性或碱性,亚铁离子与氢氧根离子反应,硝酸根离子在酸性溶液中具有强氧化性,能够氧化亚铁离子,且加入铝反应不会生成氢气.
解答 解:A.滴入甲基橙试液显红色的溶液为酸性溶液,溶液中存在大量氢离子,Mg2+、Al3+、Br-、SO42-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液中存在大量氢离子,ClO-、I-之间发生氧化还原反应,ClO-与氢离子结合生成次氯酸,在溶液中不能大量共存,故B错误;
C.NaHCO3、Ba2+、OH-之间反应生成碳酸钡沉淀,在溶液中不能大量共存,故C错误;
D.加入铝粉放出大量H2的溶液中存在大量氢离子或氢氧根离子,Fe2+与氢氧根离子反应,NO3-在酸性条件下能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
19. 氮、磷、砷是原子序数依次增大的第VA族元素,它们的化合物有着独特的性质和重要用途.
氮、磷、砷是原子序数依次增大的第VA族元素,它们的化合物有着独特的性质和重要用途.
(1)基态砷原子的核外电子排布式为[Ar]3d104s24p3.氮、磷、砷的第一电离能顺序为N>P>As(填元素符号).
(2)已知N2O为直线形结构,结构式为N=N=O.则N2O是极性(填“极性”或“非极性”)分子.中间的氮原子杂化轨道类型为sp杂化.
(3)已知下列数据:
NH3的熔、沸点均高于PH3的原因是氨分子之间能形成氢键;PH3的分解温度高于其沸点,其原因是PH3分解需要破坏P-H键,PH3气化需要破坏分子间作用力,而化学键比分子间作用力强得多.
(4)根据价层电子对互斥理论,氨分子中的键角<(填“>”“<”或“=”)109°28°;PO43-离子的空间构型为正四面体.
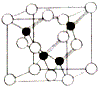
(5)磷化铝的结构与金刚石相似,其结构单元如图所示:经过计算,该晶体的化学式是AlP.
 氮、磷、砷是原子序数依次增大的第VA族元素,它们的化合物有着独特的性质和重要用途.
氮、磷、砷是原子序数依次增大的第VA族元素,它们的化合物有着独特的性质和重要用途.(1)基态砷原子的核外电子排布式为[Ar]3d104s24p3.氮、磷、砷的第一电离能顺序为N>P>As(填元素符号).
(2)已知N2O为直线形结构,结构式为N=N=O.则N2O是极性(填“极性”或“非极性”)分子.中间的氮原子杂化轨道类型为sp杂化.
(3)已知下列数据:
| 物质 | 熔点/℃ | 沸点/℃ | 分解温度/℃ |
| NH3 | 195.3 | 239.7 | 107.3 |
| PH3 | 139.2 | 185.4 | 713.2 |
(4)根据价层电子对互斥理论,氨分子中的键角<(填“>”“<”或“=”)109°28°;PO43-离子的空间构型为正四面体.
(5)磷化铝的结构与金刚石相似,其结构单元如图所示:经过计算,该晶体的化学式是AlP.
8.有A、B、C、D、E五种短周期元素,其元素特征信息如表:
回答下列问题:
(1)写出下列元素的名称:A氢、B氧、C钠、D铝、E氯;
(2)写出A、B、C形成的化合物M的化学式NaOH;
(3)写出A、B、C形成的化合物M的电子式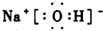 .
.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构, 且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)写出下列元素的名称:A氢、B氧、C钠、D铝、E氯;
(2)写出A、B、C形成的化合物M的化学式NaOH;
(3)写出A、B、C形成的化合物M的电子式
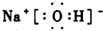 .
.
15.下列过程中,共价键被破坏的是( )
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水
⑤冰融化 ⑥NH4Cl“升华”⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水.
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水
⑤冰融化 ⑥NH4Cl“升华”⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水.
| A. | ①④⑥⑦ | B. | ④⑥⑧ | C. | ①②④⑤ | D. | ④⑥ |
5.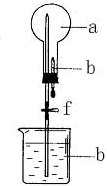 在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b不满足题目要求的是( )
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b不满足题目要求的是( )
 在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b不满足题目要求的是( )
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b不满足题目要求的是( )| a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | 4mol/LNaOH溶液 |
| C | Cl2 | 饱和NaOH溶液 |
| D | NH3 | 1mol/L盐酸 |
| A. | A | B. | B | C. | C | D. | D |
12.下列表达方式错误的是( )
| A. | 氢有三种核素:H、D、T | B. | S2-的结构示意图: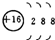 | ||
| C. | 石英中存在SiO2分子 | D. | CO2分子的结构式:O=C=O |
9.设阿伏加德罗常数为NA,下列说法正确的是( )
| A. | 18.8g苯酚中含有碳碳双键的个数为0.6NA | |
| B. | 17g羟基(-OH)所含有的电子数是10NA | |
| C. | 标准状况下,11.2L 三氯甲烷所含分子数为0.5NA | |
| D. | 常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA |
10.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样,若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5的酸碱性为酸性,试样的pH=4.
(2)为减少SO2的排放,可洗涤含SO2的烟气,下列物质可作洗涤剂的是ab(填字母)
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,简述该设想能否实现的依据)①②△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样本用蒸馏水处理制成待测试样,若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,可洗涤含SO2的烟气,下列物质可作洗涤剂的是ab(填字母)
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,简述该设想能否实现的依据)①②△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
 在某密闭容器中进行 以下反应:M(g)+N(g)?R(g)+2L(?),且此反应符合如图所示图象.图中R%表示R在平衡混合物中的含量,T1、T2表示体系温度,P1、P2表示体系压强.请判断
在某密闭容器中进行 以下反应:M(g)+N(g)?R(g)+2L(?),且此反应符合如图所示图象.图中R%表示R在平衡混合物中的含量,T1、T2表示体系温度,P1、P2表示体系压强.请判断