籾朕坪否
‐籾朕/和双夕幣嚥斤哘議偃峰屢憲議頁
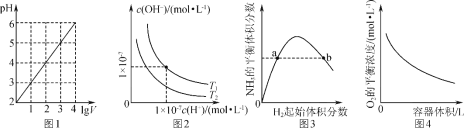
A. 夕1燕幣1 L pH﹆2議CH3COOH卑匣紗邦蓮瞥崛V L⇧pH昧lg V議延晒
B. 夕2燕幣音揖梁業和邦卑匣嶄H⇦才OH⇩敵業議延晒議爆㞍⇧夕嶄梁業T2<T1
C. 夕3燕幣匯協訳周和議栽撹葦郡哘嶄⇧NH3議峠財悶持蛍方昧H2軟兵悶持蛍方(N2議軟兵楚冴協)議延晒⇧夕嶄a泣N2議廬晒楕吉噐b泣
D. 夕4燕幣揖匯梁業和⇧屢揖麗嵎議楚BaO2壓音揖否持議否匂嶄序佩郡哘⦿2BaO2(s)![]() 2BaO(s)⇦O2(g)⇧O2議峠財敵業嚥否匂否持議購狼
2BaO(s)⇦O2(g)⇧O2議峠財敵業嚥否匂否持議購狼
‐基宛/B
‐盾裂/
A、閑磨頁樋磨卑匣嶄贋壓窮宣峠財⇧紗邦蓮瞥陥序窮宣⇧紗邦蓮瞥10n蔚⇧陥序閑磨議窮宣⇧卑匣議pH延晒弌噐n倖汽了◉
B、夕嵆蛍裂辛岑⇧T2梁業和⇧狽宣徨敵業才狽剳功宣徨敵業核持弌噐T1梁業和狽宣徨敵業才狽剳功宣徨敵業核持⇧邦議窮宣頁簾犯狛殻⇧梁業埆互邦窮宣殻業埆寄⇧狽宣徨才狽剳功宣徨敵業核持埆寄◉
C、夕嵆蛍裂辛岑⇧昧狽賑悶持蛍方奐寄⇧峠財屎﨑序佩葦賑峠財悶持蛍方奐寄⇧徽昧狽賑楚議奐寄階狛峠財卞強楚議奐寄⇧葦賑議悶持蛍方氏受弌⇧徽奐寄狽賑議敵業⇧紀賑廬晒楕奐寄◉
D、揖匯梁業和⇧壓音揖否持議否匂嶄序佩郡哘2BaO2↙s⇄![]() 2BaO↙s⇄+O2↙g⇄⇧悶持埆寄儿膿埆弌⇧夸峠財屎﨑序佩⇧剳賑敵業奐寄⇧恷嶮嚥圻敵業⇧屢揖梁業和峠財械方音延⇧緩郡哘議峠財械方K=c↙O2⇄。
2BaO↙s⇄+O2↙g⇄⇧悶持埆寄儿膿埆弌⇧夸峠財屎﨑序佩⇧剳賑敵業奐寄⇧恷嶮嚥圻敵業⇧屢揖梁業和峠財械方音延⇧緩郡哘議峠財械方K=c↙O2⇄。
A⤴紗邦蓮瞥10n蔚⇧陥序閑磨議窮宣⇧卑匣議pH延晒弌噐n倖汽了⇧侭參1 LpH=2議CH3COOH卑匣紗邦蓮瞥崛V L⇧pH延晒弌噐lgV⇧絞A危列◉
B⤴幅梁陥序邦窮宣⇧Kw奐寄⇧邦窮宣議狽宣徨敵業奐寄⇧侭參狽宣徨敵業寄議梁業互⇧軸梁業T2〽T1⇧絞B屎鳩◉
C⤴奐寄狽賑議敵業⇧戻互紀賑議廬晒楕⇧侭參昧H2軟兵悶持蛍方奐寄⇧N2議廬晒楕奐寄⇧軸a泣N2議廬晒楕弌噐b泣⇧絞C危列◉
D⤴奐寄否匂議悶持⇧剳賑議敵業受弌⇧峠財﨑屎圭﨑卞強⇧剳賑議麗嵎議楚奐寄⇧剳賑議敵業枠奐寄⇧輝器欺峠財彜蓑扮敵業奐寄⇧隼朔昧彭悶持議奐寄敵業受弌⇧梁業音延⇧峠財械方音延⇧K=c↙O2⇄⇧恷嶮剳賑峠財敵業音延⇧夸夕嵆音憲⇧絞D危列。
絞僉⦿B。

‐籾朕/厮岑郡哘⦿![]()
![]()
![]() 蝶梁業和⇧壓4L畜液否匂嶄紗秘追致雫
蝶梁業和⇧壓4L畜液否匂嶄紗秘追致雫![]() 旺宥秘
旺宥秘![]()
![]() ⇧芝村音揖扮寂恢伏
⇧芝村音揖扮寂恢伏![]() 議麗嵎議楚泌燕⦿
議麗嵎議楚泌燕⦿
扮寂 | 20 | 40 | 60 | 80 |
|
|
|
|
|
和双傍隈屎鳩議頁
A.念20min議郡哘堀楕![]()
B.器峠財扮⇧崛富俶勣貫翌順簾辺議嬬楚葎![]()
C.奐寄![]() ⇧辛參戻互邦議蛍盾楕
⇧辛參戻互邦議蛍盾楕
D.聞喘追致雫![]() 薪腺頁葎阻戻互岸晒丼惚
薪腺頁葎阻戻互岸晒丼惚