题目内容
【题目】双氧水(过氧化氢)常用于消毒、杀菌、漂白等。某化学兴趣小组同学,围绕着过氧化氢开展了调査研究与实验。
I.调查
(1)过氧化氢常用于消毒、杀菌、漂白等方面的主要原因是________。
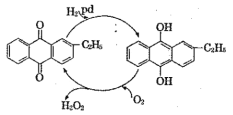
(2)制备过氧化氢目前最常用的是乙基蒽醌法,其主要过程可以用如图表示,此过程中总反应式为________。
Ⅱ.不稳定性实验研究
(3)为了探究温度、催化剂等外界条件对 H2O2的分解速率的影响,某兴趣小组同学设计了如下三组实验,部分实验数据已经填在下面表中。
实验编号 | T/X | H2O2初始浓度/mol·L-1 | FeCl3初始浓度/mol·L-1 |
I | 20 | 1.0 | _______ |
II | 50 | 1.0 | 0 |
III | 50 | ___________ | 0.1 |
实验I、Ⅱ研究______对分解速率的影响,实验Ⅱ、Ⅲ研究催化剂对分解速率的影响,则实验Ⅲ中H2O2初始浓度应为________mol·L-1。
III.过氧化氢含量的实验测定
兴趣小组同学用0.1000mol·L-1酸性高锰酸钾标准溶液滴定试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+=2Mn2+ +8H2O+5O2↑
(4)用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
计算试样中过氧化氢的浓度为________mol·L-1(保留三位有效数字)。
【答案】过氧化氢具有强氧化性 H2+O2![]() H2O2 温度 1.0 0.180
H2O2 温度 1.0 0.180
【解析】
(1)过氧化氢具有强氧化性;
(2)乙基蒽醌作催化剂,氢气和氧气反应生成双氧水;;
(3)①实验Ⅰ、Ⅱ,只有温度不同;实验Ⅱ、Ⅲ研究催化剂对分解速率的影响,则浓度相同;
②先比较温度,温度低的反应速率慢;
(4)由表中数据可知,第一次误差大可舍弃,其它三次的平均体积为18.00mL,结合反应计算。
(1)过氧化氢常用于消毒、杀菌、漂白等利用了过氧化氢的性质是强氧化性;
(2)通过图示可知,用乙基蒽醌作催化剂制取双氧水,反应为:H2+O2![]() H2O2;
H2O2;
(3)实验Ⅰ、Ⅱ研究温度对分解速率的影响,实验Ⅱ、Ⅲ是研究催化剂对分解速率的影响,物质的浓度相同,则实验Ⅲ中H2O2初始浓度应为1.0moL/L;
(4)由表中数据可知,第一次误差大可舍弃,其它三次的平均体积为18.00mL,由2MnO4-+5H2O2+6H+=2Mn2+ +8H2O+5O2↑可知,过氧化氢的浓度c(H2O2)=![]() c(MnO4-)=
c(MnO4-)=![]() ×
×![]() =0.180mol/L。
=0.180mol/L。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】(I)下表是25℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为__。
(2)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是(填“>”、“<”或“=”):CH3COOK_____NaClO,两溶液中:[c(Na+)-c(ClO-)]_____[c(K+)-c(CH3COO-)]。
(3)碳酸钠溶液中滴加少量氯水的离子方程式为__________。
(II)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
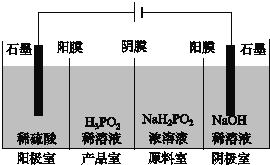
(4)写出阳极的电极反应式_________。
(5)分析产品室可得到H3PO2的原因___________。