题目内容
5.下列各组混合物中,可用过滤法进行分离的是( )| A. | 碘和四氯化碳 | B. | AgCl和水 | ||
| C. | 一氧化碳和二氧化碳 | D. | 铁粉和铜粉 |
分析 能用过滤的方法分离,则两种混合物中应存在一种不溶于水的物质,以此解答该题.
解答 解:A.碘和四氯化碳混溶,可用蒸馏的方法分离,故A错误;
B.氯化银不溶于水,可用过滤的方法分离,故B正确;
C.一氧化碳和二氧化碳为气体,可用洗气的方法分离,故C错误;
D.铁粉和铜粉都不溶于水,可用磁铁分离,故D错误.
故选B.
点评 本题考查物质的分离、提纯,为高频考点,题目侧重学生的分析、实验能力的考查,注意把握物质的性质的异同,难度不大.

练习册系列答案
相关题目
15.利用金属的活泼性不同,冶炼镁、铁、汞分别应采用的方法是( )
| A. | 热还原法、热分解法、电解法 | B. | 电解法、热还原法、热分解法 | ||
| C. | 热分解法、热还原法、电解法 | D. | 电解法、热分解法、热还原法 |
13.在标准状况下进行甲、乙、丙三组实验.各取30mL同浓度的盐酸溶液,加入不同质量的同一种镁铝合金粉末,产生气体.有关数据记录如表:
试回答:
(1)盐酸一定过量的是(填序号)甲,盐酸一定不足量的是乙和丙;
(2)要计算合金中镁的质量分数,所提供的数据中作计算依据的是甲,镁在合金中的质量分数为53.3%;
(3)在丙组实验之后,向容器中加入1mol/L的苛性钠溶液,可恰好使铝元素全部以偏铝酸根形式存在,并使镁离子
刚好沉淀完全,则溶液中偏铝酸钠的物质的量为0.009mol,所加入的苛性钠溶液的体积为39mL.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量g | 0.255 | 0.385 | 0.459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)盐酸一定过量的是(填序号)甲,盐酸一定不足量的是乙和丙;
(2)要计算合金中镁的质量分数,所提供的数据中作计算依据的是甲,镁在合金中的质量分数为53.3%;
(3)在丙组实验之后,向容器中加入1mol/L的苛性钠溶液,可恰好使铝元素全部以偏铝酸根形式存在,并使镁离子
刚好沉淀完全,则溶液中偏铝酸钠的物质的量为0.009mol,所加入的苛性钠溶液的体积为39mL.
10.下列各组中的离子,能在溶液中大量共存的是( )
| A. | H+、Mg2+、OH-、Cl- | B. | H+、Na+、SO42-、CO32- | ||
| C. | K+、Ag+、Cl-、NO3- | D. | Ca2+、K+、Cl-、NO3- |
17.我国是一个淡水资源比较匮乏的国家,下列方法能直接从海水制取可饮用水的是( )
| A. | 萃取 | B. | 结晶 | C. | 蒸馏 | D. | 过滤 |
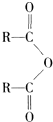 $\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH
$\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH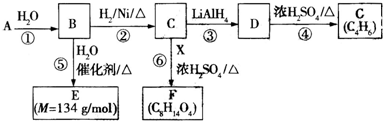
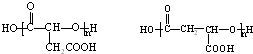 (一种即可).
(一种即可).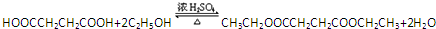 .
. .Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式:
.Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式: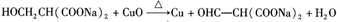 .
.