题目内容
15.利用金属的活泼性不同,冶炼镁、铁、汞分别应采用的方法是( )| A. | 热还原法、热分解法、电解法 | B. | 电解法、热还原法、热分解法 | ||
| C. | 热分解法、热还原法、电解法 | D. | 电解法、热分解法、热还原法 |
分析 根据金属活动性顺序表,金属的冶炼方法可以分为:电解法(电解熔融的化合物)、热还原法和热分解法,据此分析.
解答 解:根据金属活动性顺序表,金属的冶炼方法可以分为:K、Ca、Na、Mg、Al的冶炼用电解法(电解熔融的化合物);Zn、Fe、Sn、Pb、Cu的冶炼用热还原法;Ag、Hg的冶炼用热分解法.从而可知,冶炼镁是用电解法,电解熔融的氯化镁,冶炼铁使用热还原法,冶炼汞用的是热分解法,故选B.
点评 本题考查了金属的冶炼方法,根据金属活动性顺序表来熟练掌握金属的冶炼方法是解题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列物质的性质比较,正确的是( )
| A. | 酸性:H2SO4>HClO4 | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:P>S | D. | 气态氢化物稳定性:HCl>H2S |
6.下列叙述中,不正确的是( )
| A. | Al(OH)3胶体能疑凝聚水中悬浮物 | |
| B. | 铝易被氧化,但氧化生成的氧化铝具有保护内部铝的作用 | |
| C. | 铝是地壳中含量最多的金属元素 | |
| D. | Al(OH)3能溶于NaOH溶液、氨水和稀硫酸 |
3.如图为铜铁原电池示意图,下列有关说法正确的是( )
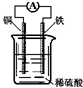

| A. | 该装置能将电能转变为化学能 | B. | 铜棒逐渐溶解 | ||
| C. | 电子由铁棒通过导线流向铜棒 | D. | 正极反应为Fe-2e-═Fe2+ |
7.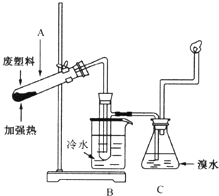 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔.

写出反应②、③的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑,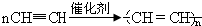 .
.
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有4种.
(3)锥形瓶C中观察到的现象是棕黄色溶液变无色或褪色,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为4.8.
(4)写出C中逸出的气体在工业上的两种用途合成氨原料、作燃料或有机化工原料.
 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 炭 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

写出反应②、③的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑,
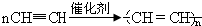 .
.(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有4种.
(3)锥形瓶C中观察到的现象是棕黄色溶液变无色或褪色,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为4.8.
(4)写出C中逸出的气体在工业上的两种用途合成氨原料、作燃料或有机化工原料.
5.下列各组混合物中,可用过滤法进行分离的是( )
| A. | 碘和四氯化碳 | B. | AgCl和水 | ||
| C. | 一氧化碳和二氧化碳 | D. | 铁粉和铜粉 |



