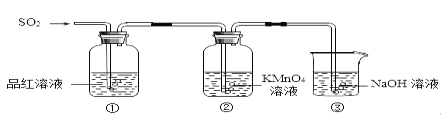
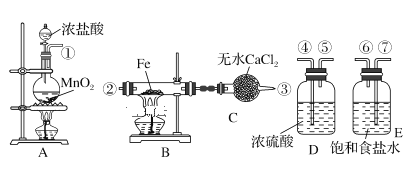
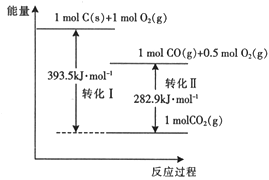
��Ŀ����
����Ŀ�������е�NO����O3Ԥ����������CaSO3����Һ����ȥ����Ԥ����ʱ������Ӧ��NO(g)��O3(g)![]() NO2(g)��O2(g)����ã�v����k��c(NO)��c(O3)��v����k��c(NO2)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣���ݻ���Ϊ2L�ļס��������ܱ������г���һ������NO��O3�����NO�����������ʱ��ı仯��ͼ��ʾ������˵����ȷ����(����)
NO2(g)��O2(g)����ã�v����k��c(NO)��c(O3)��v����k��c(NO2)��c(O2)��k����k��Ϊ���ʳ��������¶�Ӱ�졣���ݻ���Ϊ2L�ļס��������ܱ������г���һ������NO��O3�����NO�����������ʱ��ı仯��ͼ��ʾ������˵����ȷ����(����)
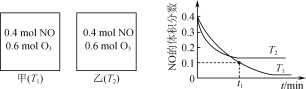
A.�������������������NO��ƽ��ת����
B.T1ʱ����Ӧ��t1min�ڵ�ƽ������v(O2)��![]() mol��L��1��min��1
mol��L��1��min��1
C.T1ʱ��NO(g)��O3(g)![]() NO2(g)��O2(g)��k����3k��
NO2(g)��O2(g)��k����3k��
D.T2ʱ����2L�ܱ������г���0.6molNO��0.4molO3������ƽ��ʱc(NO2)С����������ƽ��ʱc(NO2)
���𰸡�BC
��������
T2�¶����ȴﵽ��ѧƽ�⣬��T1��T2������ƽ��ʱ��T2�¶���NO�������������T1�¶���NO�����������˵�������¶ȣ�ƽ�������ƶ����ʸ÷�Ӧ������ӦΪ���ȷ�Ӧ��
A����Ϸ�����֪�������¶ȣ�ƽ�������ƶ���NO��ƽ��ת���ʼ�С��A����
B���ɷ�Ӧ����ʽ��֪����Ӧǰ����ϵ������������ʵ������䣬��t1ʱ��NO��С�����ʵ���=0.4mol-0.1��1mol=0.3mol������v(NO)=![]() =
=![]() mol��L��1��min��1��v(O2)=v(NO)=
mol��L��1��min��1��v(O2)=v(NO)=![]() mol��L��1��min��1��B��ȷ��
mol��L��1��min��1��B��ȷ��
C���ɷ�Ӧ����ʽ��֪����Ӧǰ����ϵ������������ʵ������䣬��ô������t1ʱ��NO��С�����ʵ���=0.4mol-0.1��1mol=0.3mol��������ʽ��

��ͼ��֪��t1ʱ��ƽ��������У�v����v������k��c(NO)��c(O3)��k��(NO2)��c(O2)��![]() ��
��![]() ��
��![]() =
=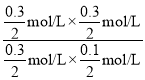 =3������
=3������![]() >3��C��ȷ��
>3��C��ȷ��
D����ƽ��ʱ��������c(NO2)=a�����ݷ���ʽ��֪c(O2)=a��c(NO)=(0.4-a)mol/L��c(O3)=(0.6-a)mol/L������ƽ�ⳣ��K=![]() �������0.6molNO��0.4molO3����ƽ��ʱc(NO2)=b����c(O2)=b��c(NO)=(0.6-b)mol/L��c(O3)=(0.4-b)mol/L��ƽ�ⳣ��K=
�������0.6molNO��0.4molO3����ƽ��ʱc(NO2)=b����c(O2)=b��c(NO)=(0.6-b)mol/L��c(O3)=(0.4-b)mol/L��ƽ�ⳣ��K=![]() ���¶Ȳ��䣬ƽ�ⳣ�����䣬����
���¶Ȳ��䣬ƽ�ⳣ�����䣬����![]() =
=![]() ������a=b�������������c(NO2)��ȣ�D����
������a=b�������������c(NO2)��ȣ�D����
��ѡBC��