题目内容
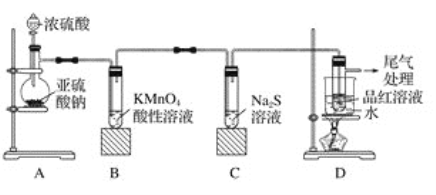
【题目】某小组同学利用如图所示装置探究二氧化硫气体的性质。
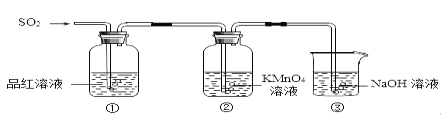
请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是_________。
(2)当观察到②中溶液颜色变浅时,①中的现象是_________。
(3)装置③的作用是________。
(4)①、②中的现象说明二氧化硫具有的性质是_________。
(5)③中涉及的化学反应方程式是_________。
【答案】Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 品红溶液褪色(或变浅) 吸收未反应的SO2,防止污染环境 漂白性、还原性 SO2+2NaOH=Na2SO3+H2O
CuSO4+SO2↑+2H2O 品红溶液褪色(或变浅) 吸收未反应的SO2,防止污染环境 漂白性、还原性 SO2+2NaOH=Na2SO3+H2O
【解析】
Cu与浓硫酸混合加热反应产生SO2,SO2具有漂白性,能够使品红溶液褪色;SO2具有还原性,能够被酸性KMnO4溶液氧化使溶液的紫色褪色;SO2为酸性氧化物,也是大气污染物,可以与NaOH溶液反应产生Na2SO3,因此用NaOH溶液吸收尾气中的SO2。
(1)在实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)当观察到②中溶液颜色变浅时,说明有SO2气体通过品红溶液,由于SO2气体有漂白性,因此可以使品红溶液褪色,因此①中的现象是品红溶液褪色(或溶液颜色变浅);
(3)NaOH是碱,可以与酸性氧化物SO2反应,所以装置③的作用是吸收未反应的SO2,防止污染环境;
(4)①褪色说明SO2具有漂白性;②中溶液颜色变浅说明二氧化硫具有还原性,因此①、②中的现象说明二氧化硫具有的性质是漂白性、还原性;
(5)③中SO2与NaOH反应产生Na2SO3和H2O,涉及的化学反应方程式是SO2+2NaOH=Na2SO3+H2O。

【题目】氨的合成原理为:N2(g)+3H2(g)2NH3(g)H=-92.4kJ·mol-1在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图。回答下列问题:
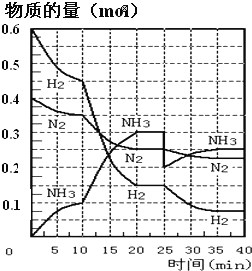
(1)10min内以NH3表示的平均反应速率为_________
(2)在10~20min内,NH3浓度变化的原因可能是_____________
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡:平衡常数K1=__________(带数据的表达式),第2次平衡时NH3的体积分数为_____________。
(4)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fc2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)2NH3+1.5O2(g)H=akJ·mol-1,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a______0,△S_______0;(填“>”、“<”或一”)
②已知N2(g)+3H2(g)2NH3(g)H=-92.4kJ·mol-1,2 H2(g)+ O2(g)=2H2O(l)H=-571.kJ·mol-1 则常温下氮气与水反应生成氨气与氧气的热化学方程式为_____________________________