题目内容
5.判断下列反应在常温常压下能自发进行的是(1)(3)(填序号).(1)2KClO3(s)═2KCl(s)+3O2(g)△H=-78.03kJ•mol-1△S=+494.4J•mol-1•K-1
(2)CO(g)═C(s,石墨)+$\frac{1}{2}$O2(g)△H=+110.5kJ•mol-1△S=-89.36J•mol-1•K-1
(3)4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=-444.3kJ•mol-1△S=-280.1J•mol-1•K-1
(4)CaCO3(s)═CaO(s)+CO2(g)△H=+178.2kJ•mol-1△S=+169.6J•mol-1•K-1.
分析 反应自发进行的判断依据是△H-T△S<0,依据热化学方程式焓变、熵变、温度分析判断.
解答 解:常温常压下,T=298K
(1)2KClO3(s)═2KCl(s)+3O2(g)△H=-78.03kJ•mol-1△S=+494.4J•mol-1•K-1,△H-T△S=-78.03kJ•mol-1-298×0.4944KJ•mol-1•K-1=-225.3KJ/mol<0,反应自发进行,故(1)正确;
(2)CO(g)═C(s,石墨)+$\frac{1}{2}$O2(g)△H=+110.5kJ•mol-1△S=-89.36J•mol-1•K-1,△H-T△S=110.5kJ•mol-1-298K×(-0.089.36KJ•mol-1•K-1)>0,反应一定非自发进行,故(2)错误;
(3)4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=-444.3kJ•mol-1△S=-280.1J•mol-1•K-1 ,△H-T△S=-444.3kJ•mol-1-298K×(-0.2801KJ•mol-1•K-1 )=-360.8KJ/mol<0,反应自发进行,故(3)正确;
(4)CaCO3(s)═CaO(s)+CO2(g)△H=+178.2kJ•mol-1△S=+169.6J•mol-1•K-1,△H-T△S=178.2kJ•mol-1-298K×0.1696KJ•mol-1•K-1=127.7KJ/mol>0,故(4)错误;
故答案为:(1)(3).
点评 本题考查了反应自发进行的判断依据,依据焓变、熵变、温度的计算是解题关键,题目较简单.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
20.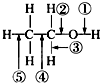 乙醇分子中的各种化学键如图所示,下列关于乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子中的各种化学键如图所示,下列关于乙醇在各种反应中断裂键的说明不正确的是( )
 乙醇分子中的各种化学键如图所示,下列关于乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子中的各种化学键如图所示,下列关于乙醇在各种反应中断裂键的说明不正确的是( )| A. | 和金属钠反应时①键断裂 | |
| B. | 和乙酸发生酯化反应时②键断裂 | |
| C. | 在铜催化及加热条件下与O2反应时断裂①键和⑤键 | |
| D. | 在空气中完全燃烧时断裂①②③④⑤键 |
16.既能用来鉴别甲烷与乙烯,又能用来除去甲烷中的乙烯以提纯甲烷的方法是( )
| A. | 通过足量的NaOH溶液 | B. | 通过足量的溴水 | ||
| C. | 在Ni催化、加热条件下通入H2 | D. | 通过足量的酸性KMnO4溶液 |
13.下列各组离子在指定条件下一定能大量共存的是( )
| A. | 加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- | |
| B. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:Na+、CO32-、NO3-、AlO2- | |
| C. | 无色溶液中:K+、AlO2-、HCO3-、Cr2O72- | |
| D. | pH=1的溶液中:Na+、Al3+、NO3-、S2O32- |
17.通常情况下能共存且能用浓硫酸干燥的气体组是( )
| A. | NH3、H2 | B. | NH3、HCl | C. | NO、O2 | D. | N2、O2 |
14.用铂电极电解某金属的氯化物(MCl2)溶液,当阳极上收集到1.12LCl2时(标准状况),阴极增重3.2g.下列有关叙述正确的是( )
| A. | M的相对原子质量为32 | B. | M的相对原子质量为64 | ||
| C. | 电解过程中溶液的pH不发生变化 | D. | 电路中通过0.05mol电子 |
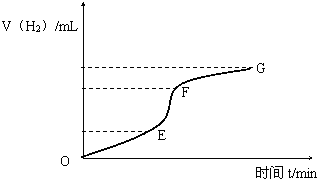 用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答: