题目内容
5.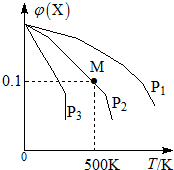 某可逆反应为2X(g)═3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
某可逆反应为2X(g)═3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )| A. | 升高温度,该反应平衡常数K减小 | B. | 压强大小有P3>P2>P1 | ||
| C. | 平衡后加入高效催化剂使Mr增大 | D. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ |
分析 A、根据图象中升高温度X转化率降低确定反应的移动方向,进而确定平衡常数的变化;
B、减小压强,可逆反应向着气体分子数增大的反应方向进行;
C、催化剂不会使平衡发生移动;
D、M点X的物质的量分数为0.1,根据化学平衡的三行式计算物质的转化率.
解答 解:A、根据图象知,升高温度,X转化率降低,说明反应向正方向移动,平衡常数增大,故A错误;
B、可逆反应的正反应是气体分子数增大的反应,减小压强,X转化率增大,所以,压强大小关系有:P3<P2<P1,故B错误;
C、催化剂不会使平衡发生移动,气体相对分子质量Mr不变,故C错误;
D、M点对应的平衡体系中,X的体积分数为0.1,则
2X(g) 3Y(g)+Z(g)
3Y(g)+Z(g)
起始:1 0 0
平衡:1-2x x 3x
$\frac{1-2x}{1+2x}$=0.1,x=$\frac{9}{22}$,X转化率为$\frac{2x}{1}$=$\frac{2×9}{22}$=$\frac{9}{11}$,故D正确.
故选D.
点评 本题涉及化学平衡移动原理、化学平衡的有关计算等方面的知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
16.下列表示物质的化学用语或模型正确的是( )
| A. | 羟基的电子式: | B. | CH4分子的比例模型: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 1,2-二甲基丁烷的结构简式为: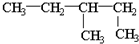 |
13.某碳、氢、氧有机物的蒸气密度是CO2的2倍(相同条件),它含有“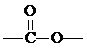 ”的同分异构体有( )
”的同分异构体有( )
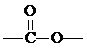 ”的同分异构体有( )
”的同分异构体有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
20.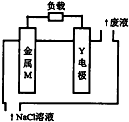 锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中.某金属燃料电池的基本结构如图所示,其中Y电极为石墨.下列说法正确的是( )
锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中.某金属燃料电池的基本结构如图所示,其中Y电极为石墨.下列说法正确的是( )
 锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中.某金属燃料电池的基本结构如图所示,其中Y电极为石墨.下列说法正确的是( )
锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中.某金属燃料电池的基本结构如图所示,其中Y电极为石墨.下列说法正确的是( )| A. | 该电池工作时,电子沿M→电解液→Y电极流动 | |
| B. | 若M为铝,则该电池工作时溶液的pH将不断增大 | |
| C. | 若M为镁,则该电池反应的化学方程式为2Mg+O2=2MgO | |
| D. | 若M为铁,则该电池工作时负极发生的反应为Fe-2e-=Fe2+ |
17.25℃时,下列溶液的离子浓度关系式正确的是( )
| A. | pH=a的醋酸溶液稀释10倍后,其pH=b,则b=a+1 | |
| B. | 浓度相同的①NH4Cl;②CH3COONH4;③NH4HSO4三种溶液的c(NH4+):①>③>② | |
| C. | 浓度相同的氨水与盐酸等体积混合:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| D. | 将amol•L-1CH3COOH与bmol•L-1NaOH溶液等体积混合,测得溶液pH为7,则a>b |
14.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| C. | PM2.5含有的铅、铬、钒、砷等对人体有害的金属元素 | |
| D. | 煤、石油、天然气是一级能源 |
15.如图为元素周期表短周期的一部分.其中W元素的最高正价与最低负价的代数和为4.下列有关说法正确的是( )
| X | |||
| Z | Y | W |
| A. | X、Y、W的氧化物都属于酸性氧化物 | |
| B. | 工业上采用电解Z的氯化物制备Z单质 | |
| C. | W的单质易溶于XW2 | |
| D. | 1molX或Y的最高价氧化物分子中都含有2mol双键 |
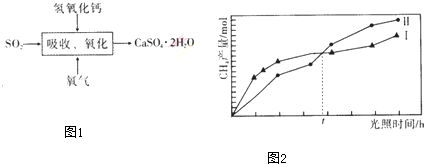
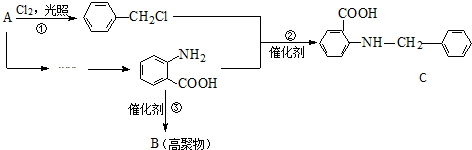
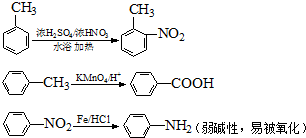
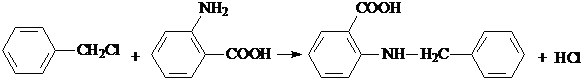 .
.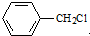 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,写出X所有的可能结构简式:
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,写出X所有的可能结构简式: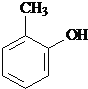 、
、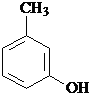 、
、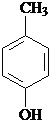 .
.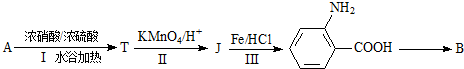
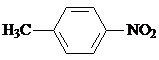 .
.