题目内容
6.低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是( )| A. | 工业上利用热还原法冶炼金属Fe、Cr、Mn | |
| B. | Fe位于元素周期表的第四周期、第ⅧB族 | |
| C. | ${\;}_{22}^{46}$TiO2、${\;}_{22}^{48}$TiO2、${\;}_{22}^{50}$TiO2互为同位素 | |
| D. | ${\;}_{41}^{92}$Nb3+原子核内有51个中子,核外有44个电子 |
分析 A.Fe、Cr、Mn单质的熔点大于Al,且金属性小于Al,可以采用铝热反应冶炼Fe、Cr、Mn;
B.Fe位于第四周期第VIII族;
C.质子数相同、中子数不同的同一元素不同原子互称同位素;
D.原子符号左下角数字是质子数、左上角数字是质量数,阳离子中核外电子数=质子数-电荷数.
解答 解:A.Fe、Cr、Mn单质的熔点大于Al,且金属性小于Al,可以采用铝热反应冶炼Fe、Cr、Mn,属于热还原法,故A正确;
B.Fe位于第四周期第VIII族,与其同一周期同一族的还有Co、Ni,故B错误;
C.质子数相同、中子数不同的同一元素不同原子互称同位素,这几种微粒都不是原子,所以不是同位素,故C错误;
D.原子符号左下角数字是质子数、左上角数字是质量数,阳离子中核外电子数=质子数-电荷数=41-3=38,故D错误;
故选A.
点评 本题考查金属冶炼、元素在周期表中的位置、同位素等知识点,侧重考查基本概念及金属冶炼方法,会根据金属活泼性强弱选取合适的冶炼方法,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
16.下列有机物分子中,所有的原子不可能处于同一平面的是( )
| A. | CH2=CH-CI | B. | CH2=CH-CH=CH2 | C. | CH3-CH=CH2 | D. | 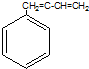 |
17.将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中充分反应后,放出氢气最多的是( )
| A. | 3mol/LHCl | B. | 4mol/LHNO3 | C. | 8mol/LNaOH | D. | 18mol/LH2SO4 |
14.下列关于常见有机物的说法不正确的是( )
| A. | 乙烯和甲烷可用酸性高锰酸钾溶液鉴别 | |
| B. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| C. | 2-戊烯存在顺反异构现象 | |
| D. | 乙烯和苯都能与酸性高锰酸钾溶液、溴水反应 |
1. 下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
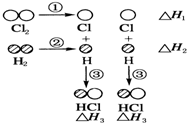
H2和Cl2反应生成HCl过程中的热效应可用如图表示,请回答下列问题:
(1)△H1=+243kJ•mol-1,△H2=+436kJ•mol-1,△H3=-431kJ•mol-1.
(2)该反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ•mol-1.
 下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能/kJ•mol-1 | 436 | 243 | 431 |
(1)△H1=+243kJ•mol-1,△H2=+436kJ•mol-1,△H3=-431kJ•mol-1.
(2)该反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ•mol-1.
11.下列事实中,不能用勒夏特列原理解释的是( )
| A. | 高压有利于氨的合成 | |
| B. | 实验室中常用排饱和食盐水的方式收集氯气 | |
| C. | 打开汽水瓶,有气泡从溶液中冒出 | |
| D. | 向双氧水中加入二氧化锰有利于氧气的生成 |
13.达到化学平衡的条件是( )
| A. | 逆反应停止 | B. | 正逆反应速率相等 | ||
| C. | 反应停止产生热 | D. | 反应物与产物浓度相等 |
 2SO2(g)+O2(g);△H =+196.6 kJ/mol
2SO2(g)+O2(g);△H =+196.6 kJ/mol