题目内容
17.将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中充分反应后,放出氢气最多的是( )| A. | 3mol/LHCl | B. | 4mol/LHNO3 | C. | 8mol/LNaOH | D. | 18mol/LH2SO4 |
分析 Mg、Al都和稀盐酸反应生成氢气,都和稀硝酸反应生成NO,只有Al和NaOH反应生成氢气,常温下Al和浓硫酸发生钝化现象且镁和浓硫酸反应生成二氧化硫,据此分析解答.
解答 解:A.Mg和Al都和稀盐酸反应生成氯化物和氢气;
B.Mg、Al和稀硝酸反应分别生成硝酸盐和NO,没有氢气生成;
C.只有Al和NaOH反应生成氢气,且铝的物质的量相同,铝和足量稀盐酸、NaOH溶液反应生成氢气物质的量相同,Mg和NaOH溶液不反应,所以生成的氢气量小于A;
D.常温下,浓硫酸和Al发生钝化现象且生成二氧化硫而不是氢气,镁和浓硫酸反应生成二氧化硫而不是氢气,生成氢气的量为0;
通过以上分析知,生成氢气的量最多的是A,故选A.
点评 本题以金属为载体考查化学方程式有关计算,侧重考查学生分析判断能力,明确金属性质是解本题关键,注意BD中不生成氢气,为易错点.

练习册系列答案
相关题目
8.下列措施对增大反应速率明显有效的是( )
| A. | 在炭粉燃烧中加入KClO3 | |
| B. | Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 | |
| C. | 在K2S04与BaCl2两溶液反应时,增大压强 | |
| D. | Na与乙醇反应时增大乙醇的用量 |
12.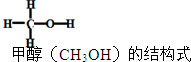 已知:2H2(g)+CO(g)═CH3OH(g)△H=-90kJ/mol,其他相关数据如表
已知:2H2(g)+CO(g)═CH3OH(g)△H=-90kJ/mol,其他相关数据如表
则CO中碳氧键的键能为( )
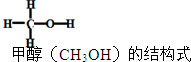 已知:2H2(g)+CO(g)═CH3OH(g)△H=-90kJ/mol,其他相关数据如表
已知:2H2(g)+CO(g)═CH3OH(g)△H=-90kJ/mol,其他相关数据如表| 共价键 | H-H | C-H | C-O | O-H |
| 键能(kJ/mol) | 436 | 414 | 326 | 464 |
| A. | 1070 kJ/mol | B. | 1080 kJ/mol | C. | 1090 kJ/mol | D. | 1100 kJ/mol |
2.下列实验方案的设计中,不正确的是( )
| A. | 用灼烧法鉴别羊毛纤维和棉纤维 | |
| B. | 用适量稀硫酸清除铁制品表面的铁锈 | |
| C. | 用适量熟石灰除去氯化钠溶液中少量的碳酸钠 | |
| D. | 用足量稀盐酸检验久置的氢氧化钠固体是否变质 |
9.下列说法中,正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 燃煤发电是煤的综合利用的重要途径 | |
| C. | 反应物的总能量大于生成物的总能量的化学反应是放热反应 | |
| D. | 化学键的断裂和形成与化学变化中的能量变化无关 |
6.低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是( )
| A. | 工业上利用热还原法冶炼金属Fe、Cr、Mn | |
| B. | Fe位于元素周期表的第四周期、第ⅧB族 | |
| C. | ${\;}_{22}^{46}$TiO2、${\;}_{22}^{48}$TiO2、${\;}_{22}^{50}$TiO2互为同位素 | |
| D. | ${\;}_{41}^{92}$Nb3+原子核内有51个中子,核外有44个电子 |
4.对于下列常见化学的认识错误的是( )
| A. | 明矾可用作净水剂 | |
| B. | 干冰能用于人工降雨 | |
| C. | 小苏打是一种膨松剂,可用于制作馒头和面包 | |
| D. | 碳酸钙是文物陶瓷的主要成分 |
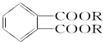 (其中R为烃基),实验室由以下方法可得到DMP:
(其中R为烃基),实验室由以下方法可得到DMP: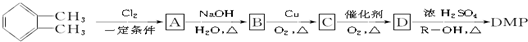
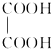 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为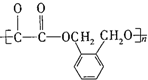 .
.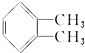 )为原料先生产苯酐(
)为原料先生产苯酐(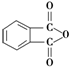 ),再使其与某醇在一定条件下反应制取DMP.苯酐与该醇制取DMP的化学方程式为
),再使其与某醇在一定条件下反应制取DMP.苯酐与该醇制取DMP的化学方程式为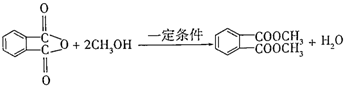 .
.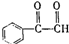 .B也存在多种同分异构体,符合下列条件的B同分异构体有6种.
.B也存在多种同分异构体,符合下列条件的B同分异构体有6种.