题目内容
14.下列关于常见有机物的说法不正确的是( )| A. | 乙烯和甲烷可用酸性高锰酸钾溶液鉴别 | |
| B. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| C. | 2-戊烯存在顺反异构现象 | |
| D. | 乙烯和苯都能与酸性高锰酸钾溶液、溴水反应 |
分析 A.乙烯含有碳碳双键,可被酸性高锰酸钾氧化;
B.羧基、酯基都可与氢氧化钠反应;
C.2-戊烯为CH3CH=CHCH2CH3,其中C=C连接不同的H、-CH3、-CH2CH3,具有顺反异构;
D.苯与高锰酸钾、溴水不反应.
解答 解:A.甲烷为饱和烃,与高锰酸钾不反应,而乙烯含有碳碳双键,可被酸性高锰酸钾氧化,故A正确;
B.乙酸含有羧基,具有酸性,可与碱发生中和反应,乙酸乙酯含有酯基,可在碱性条件下水解,故B正确;
C.2-戊烯为CH3CH=CHCH2CH3,其中C=C连接不同的H、-CH3、-CH2CH3,具有顺反异构,故C正确;
D.苯性质稳定,与高锰酸钾、溴水不反应,故D错误.
故选D.
点评 本题考查较综合,涉及有机物的结构与性质、有机反应、有机物的鉴别等,侧重甲烷、乙烯、苯、油脂、乙酸性质的考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
4.a mol O2气体和a mol O3气体相比较,下列叙述一定正确的是( )
| A. | 体积相同 | B. | 质量相等 | C. | 分子数相等 | D. | 原子数相等 |
2.下列实验方案的设计中,不正确的是( )
| A. | 用灼烧法鉴别羊毛纤维和棉纤维 | |
| B. | 用适量稀硫酸清除铁制品表面的铁锈 | |
| C. | 用适量熟石灰除去氯化钠溶液中少量的碳酸钠 | |
| D. | 用足量稀盐酸检验久置的氢氧化钠固体是否变质 |
9.下列说法中,正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 燃煤发电是煤的综合利用的重要途径 | |
| C. | 反应物的总能量大于生成物的总能量的化学反应是放热反应 | |
| D. | 化学键的断裂和形成与化学变化中的能量变化无关 |
6.低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是( )
| A. | 工业上利用热还原法冶炼金属Fe、Cr、Mn | |
| B. | Fe位于元素周期表的第四周期、第ⅧB族 | |
| C. | ${\;}_{22}^{46}$TiO2、${\;}_{22}^{48}$TiO2、${\;}_{22}^{50}$TiO2互为同位素 | |
| D. | ${\;}_{41}^{92}$Nb3+原子核内有51个中子,核外有44个电子 |
20.把Ca(OH)2溶入蒸馏水中,一定时间后达到以下平衡:Ca(OH)2(s)?Ca2++2OH-,加入以下溶液,可使Ca(OH)2(s)减少的是( )
| A. | CaO | B. | AlCl3 | C. | NaOH | D. | CaCl2 |
1.下表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体.
(1)a的元素在元素周期表中的位置为第四周期第ⅦA族.
(2)写出d的元素原子的电子式 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为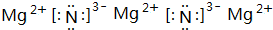 .
.
(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
| 单质 | a | b | c | d | e |
| 沸点(℃) | 58.8 | 882.9 | 444.7 | 2 355 | 1 107 |
(2)写出d的元素原子的电子式
 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为
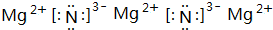 .
.(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
 联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.