题目内容
13.达到化学平衡的条件是( )| A. | 逆反应停止 | B. | 正逆反应速率相等 | ||
| C. | 反应停止产生热 | D. | 反应物与产物浓度相等 |
分析 化学平衡的实质是正逆反应速率相等,当达到平衡状态时,各物质的浓度不变,由此衍生的一些物理量也不变,即可解答该题.
解答 解:可逆反应达到平衡状态时,正逆反应速率相等,但反应没有停止,为动态平衡,达到平衡时,各物质的浓度不变,但不一定相等,只有B正确.
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大,本题注意把握平衡状态的特征以及判断的角度.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是( )
| A. | 工业上利用热还原法冶炼金属Fe、Cr、Mn | |
| B. | Fe位于元素周期表的第四周期、第ⅧB族 | |
| C. | ${\;}_{22}^{46}$TiO2、${\;}_{22}^{48}$TiO2、${\;}_{22}^{50}$TiO2互为同位素 | |
| D. | ${\;}_{41}^{92}$Nb3+原子核内有51个中子,核外有44个电子 |
4.对于下列常见化学的认识错误的是( )
| A. | 明矾可用作净水剂 | |
| B. | 干冰能用于人工降雨 | |
| C. | 小苏打是一种膨松剂,可用于制作馒头和面包 | |
| D. | 碳酸钙是文物陶瓷的主要成分 |
1.下表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体.
(1)a的元素在元素周期表中的位置为第四周期第ⅦA族.
(2)写出d的元素原子的电子式 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为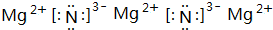 .
.
(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
| 单质 | a | b | c | d | e |
| 沸点(℃) | 58.8 | 882.9 | 444.7 | 2 355 | 1 107 |
(2)写出d的元素原子的电子式
 ;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.
;其最高价氧化物形成的晶体为原子晶体(填类型),d单质溶于强碱的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑.(3)c与氢形成的分子X的空间构型为V型;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式H2S+2OH-=S2-+H2O.
(4)上述元素所能形成的简单离子中半径最小的是Mg2+(填离子符号),最高价氧化物对应水化物酸性最强的是HBrO4(填分子式),e元素与N元素形成化合物的电子式为
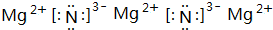 .
.(5)b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是4个Na+、4个Cl-.
18.下列微粒中,既含有离子键又含有共价键的是( )
| A. | NH3 | B. | NH4Cl | C. | H2S | D. | KCl |
5.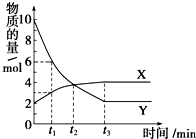 一定温度下在2L容器内进行着某一反应,固体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行着某一反应,固体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在2L容器内进行着某一反应,固体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行着某一反应,固体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为4X?Y | |
| B. | 当t1=2时,用X表示该反应在2min内的平均反应速率为0.25mol/(L•min) | |
| C. | t2时,正反应速率等于逆反应速率 | |
| D. | t3时,Y浓度不再变化,反应达到平衡 |
13.下列分子构型呈正四面体结构的是( )
①P4 ②NH3 ③CCl4 ④金刚石 ⑤CH4 ⑥SiO2 ⑦H2O ⑧CO2.
①P4 ②NH3 ③CCl4 ④金刚石 ⑤CH4 ⑥SiO2 ⑦H2O ⑧CO2.
| A. | ①③④⑤ | B. | ①③④⑤⑥ | C. | ①③⑤ | D. | ④⑤ |
 B
B