题目内容
 按要求完成下列两题:
按要求完成下列两题:I:某化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).
(1)该产品的结构简式为
(2)用核磁共振谱可以证明该化合物的核磁共振氢谱中有种吸收峰,各吸收峰面积之比为:
(3)该物质能使溴水褪色,写出该反应的方程式:
(4)下列物质中,与该产品互为同分异构体的是
①CH3CH=CHCOOH ②CH2=CHCOOCH3
③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH
Ⅱ:某含氧有机物,它的相对分子质量为74.7.4g该含氧有机物充分燃烧后的产物通过浓硫酸后增重5.4g,通过足量澄清石灰水后有30g白色沉淀生成.
(1)该含氧有机物的分子式为
(2)该含氧有机物有多种同分异构体,写出其中含有酯基的所有同分异构体的结构简式
考点:有机物的结构和性质,芳香烃、烃基和同系物,同分异构现象和同分异构体,有关有机物分子式确定的计算
专题:同系物和同分异构体,有机物的化学性质及推断,烃及其衍生物的燃烧规律
分析:I.由结构模型可知有机物的结构简式为CH2=C(CH3)COOH,含有碳碳双键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化反应;
Ⅱ.浓硫酸质量增重5.4g为燃烧生成水的质量,30g白色沉淀为碳酸钙的质量,根据n=
计算该有机物、水、碳酸钙的物质的量,根据原子守恒计算N(C)、N(H),在结合相对分子质量计算N(O),进而确定分子式,该有机物能水解的同分异构体,应含有酯基,结合有机物分子式确定该同分异构体的结构简式.
Ⅱ.浓硫酸质量增重5.4g为燃烧生成水的质量,30g白色沉淀为碳酸钙的质量,根据n=
| m |
| M |
解答:
解:I.(1)由结构模型可知有机物的结构简式为CH2=C(CH3)COOH,故答案为:CH2=C(CH3)COOH;
(2)CH2=C(CH3)COOH含有3种不同的H,个数比为1:2:3,则峰面积之比为1:2:3,故答案为:1:2:3;
(3)含有碳碳双键,可与溴发生加成反应,方程式为CH2=C(CH3)COOH+Br2→CH2BrC(CH3)BrCOOH,
故答案为:CH2=C(CH3)COOH+Br2→CH2BrC(CH3)BrCOOH;
(4)①②与CH2=C(CH3)COOH分子式相同,但结构不同,互为同分异构体,③与 CH2=C(CH3)COOH互为同系物,
故答案为:①②;③;
Ⅱ.(1)浓硫酸质量增重5.4g为燃烧生成水的质量,水的物质的量为
=0.3mol,n(H)=0.6mol,
30g白色沉淀为碳酸钙的质量,其物质的量为
=0.3mol,n(C)=0.3mol,
7.4g该有机物的物质的量为
=0.1mol,
故该有机物分子中N(C)=
=3、N(H)=
=6,故N(O)=
=2,
故该有机物的分子式为C3H6O2,
答:该有机物的分子式为C3H6O2.
(2)该有机物能水解的同分异构体,应含有酯基,符合条件的同分异构体为CH3COOCH3、HCOOCH2CH3,
答:该有机物能水解的同分异构体的结构简式为CH3COOCH3、HCOOCH2CH3.
(2)CH2=C(CH3)COOH含有3种不同的H,个数比为1:2:3,则峰面积之比为1:2:3,故答案为:1:2:3;
(3)含有碳碳双键,可与溴发生加成反应,方程式为CH2=C(CH3)COOH+Br2→CH2BrC(CH3)BrCOOH,
故答案为:CH2=C(CH3)COOH+Br2→CH2BrC(CH3)BrCOOH;
(4)①②与CH2=C(CH3)COOH分子式相同,但结构不同,互为同分异构体,③与 CH2=C(CH3)COOH互为同系物,
故答案为:①②;③;
Ⅱ.(1)浓硫酸质量增重5.4g为燃烧生成水的质量,水的物质的量为
| 5.4g |
| 18g/mol |
30g白色沉淀为碳酸钙的质量,其物质的量为
| 30g |
| 100g/mol |
7.4g该有机物的物质的量为
| 7.4g |
| 74g/mol |
故该有机物分子中N(C)=
| 0.3mol |
| 0.1mol |
| 0.6mol |
| 0.1mol |
| 74-12×3-6 |
| 2 |
故该有机物的分子式为C3H6O2,
答:该有机物的分子式为C3H6O2.
(2)该有机物能水解的同分异构体,应含有酯基,符合条件的同分异构体为CH3COOCH3、HCOOCH2CH3,
答:该有机物能水解的同分异构体的结构简式为CH3COOCH3、HCOOCH2CH3.
点评:本题综合考查有机物的结构和性质,侧重于学生的分析能力和计算能力的考查,为高频考点,注意把握有机物的结构特点和官能团的性质,难度中等.

练习册系列答案
相关题目
下列关于元素周期律的叙述正确的是( )
| A、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| B、元素性质的周期性变化是指原子核外电子排布、原子半径及元素主要化合价的周期性变化 |
| C、随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 |
| D、在元素周期表中有些元素既表现出一定的金属性又表现出一定的非金属性 |
下列有关实验原理、方法和结论都正确的是( )
| A、向饱和FeCl3溶液中滴加过量稀氨水,可制取Fe(OH)3胶体 |
| B、向淀粉溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2,再加热,无砖红色沉淀出现,则证明淀粉没有发生水解 |
| C、常温下,向盛有2mL 0.1mol?L-1 AgNO3溶液的试管中滴加2滴同浓度的NaCl溶液,生成白色沉淀,再向其中滴加0.1mol?L-1的KI溶液又生成黄色沉淀,说明Ksp(AgI)<Ksp(AgCl) |
| D、取少量溶液X,向其中加入几滴KSCN溶液无明显变化,再加适量新制氯水溶液变红,说明X溶液中一定含有Fe2+ |




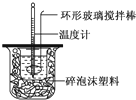
 某化学兴趣小组要完成中和热的测定.
某化学兴趣小组要完成中和热的测定.