题目内容
下列有关实验原理、方法和结论都正确的是( )
| A、向饱和FeCl3溶液中滴加过量稀氨水,可制取Fe(OH)3胶体 |
| B、向淀粉溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2,再加热,无砖红色沉淀出现,则证明淀粉没有发生水解 |
| C、常温下,向盛有2mL 0.1mol?L-1 AgNO3溶液的试管中滴加2滴同浓度的NaCl溶液,生成白色沉淀,再向其中滴加0.1mol?L-1的KI溶液又生成黄色沉淀,说明Ksp(AgI)<Ksp(AgCl) |
| D、取少量溶液X,向其中加入几滴KSCN溶液无明显变化,再加适量新制氯水溶液变红,说明X溶液中一定含有Fe2+ |
考点:化学实验方案的评价
专题:实验评价题
分析:A.反应生成沉淀;
B.水解后显酸性,应加碱至碱性,检验水解产物;
C.滴加2滴同浓度的NaCl溶液,生成白色沉淀,硝酸银过量,发生沉淀的生成;
D.加入几滴KSCN溶液无明显变化,说明不含铁离子,再加新制氯水溶液变红,说明氧化生成铁离子.
B.水解后显酸性,应加碱至碱性,检验水解产物;
C.滴加2滴同浓度的NaCl溶液,生成白色沉淀,硝酸银过量,发生沉淀的生成;
D.加入几滴KSCN溶液无明显变化,说明不含铁离子,再加新制氯水溶液变红,说明氧化生成铁离子.
解答:
解:A.向饱和FeCl3溶液中滴加过量稀氨水,生成沉淀,应向沸水中滴加饱和FeCl3溶液制取Fe(OH)3胶体,故A错误;
B.向淀粉溶液中加入稀硫酸,加热,冷却后,先加碱至碱性,再加入新制Cu(OH)2,再加热,观察是否有砖红色沉淀出现,证明淀粉是否水解,故B错误;
C.硝酸银过量,发生沉淀的生成,而不是沉淀的转化,则不能比较Ksp大小,故C错误;
D.加入几滴KSCN溶液无明显变化,说明不含铁离子,再加新制氯水溶液变红,说明氧化生成铁离子,则说明X溶液中一定含有Fe2+,故D正确;
故选D.
B.向淀粉溶液中加入稀硫酸,加热,冷却后,先加碱至碱性,再加入新制Cu(OH)2,再加热,观察是否有砖红色沉淀出现,证明淀粉是否水解,故B错误;
C.硝酸银过量,发生沉淀的生成,而不是沉淀的转化,则不能比较Ksp大小,故C错误;
D.加入几滴KSCN溶液无明显变化,说明不含铁离子,再加新制氯水溶液变红,说明氧化生成铁离子,则说明X溶液中一定含有Fe2+,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及胶体制备、水解产物检验、离子检验及沉淀生成和转化等,侧重物质性质及反应原理的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
可以证明乙醇分子中有一个氢原子与另外的氢原子不同的是( )
| A、1mol乙醇燃烧生成3mol水 |
| B、1mol乙醇可以生成1mol乙醛 |
| C、1mol乙醇跟足量的金属作用得0.5mol H2 |
| D、乙醇可以制酒精饮料 |
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
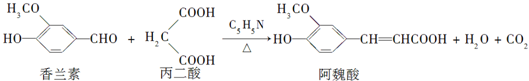
下列说法正确的是( )

下列说法正确的是( )
| A、可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
| B、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应 |
下列有关元素锗及其化合物的叙述中正确的是( )
| A、锗的第一电离能高于碳而电负性低于碳 |
| B、四氯化锗与四氯化碳分子都是四面体构型 |
| C、二氧化锗与二氧化碳都是非极性的气体化合物 |
| D、二氧化锗有强氧化性 |
下列反应属于氮的固定的是( )
| A、Cl2将NH3氧化成N2 |
| B、NH3和HCl生成NH4Cl固体 |
| C、豆科植物将N2转化为NH4+ |
| D、空气中的氮氧化物转化成酸雨 |
分子式为C4H8O2的有机物在酸性条件下可水解为羧酸和醇,若不考虑立体结构,这些醇和羧酸重新组合可形成的酯共有( )
| A、4种 | B、11种 |
| C、12种 | D、13种 |
下列实验能获得成功的是( )
| A、在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯 |
| B、用溴水可鉴别苯、CCl4、苯乙烯 |
| C、鉴定溴乙烷中存在溴元素的实验操作是先加入NaOH溶液,加热后再加入AgNO3溶液 |
| D、配制银氨溶液时,将硝酸银溶液逐滴加入到稀氨水中 |
 按要求完成下列两题:
按要求完成下列两题: