题目内容
欲将MgCl2、AlCl3的混合溶液分离,某同学设计了如下方案:
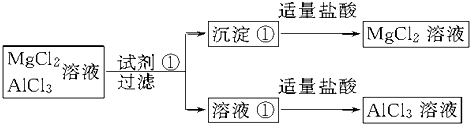
(1)试剂①应选 (填“NaOH溶液”或“氨水”).该试剂的用量是 (填“过量”或“少量”).
(2)请写出过滤后所得沉淀①的化学式 ,沉淀①需进行洗涤,洗涤沉淀的方法是 .
(3)写生成溶液①的离子方程式: .
(4)以上实验设计明显存在缺陷,请将其指出 ,怎样改进? .

(1)试剂①应选
(2)请写出过滤后所得沉淀①的化学式
(3)写生成溶液①的离子方程式:
(4)以上实验设计明显存在缺陷,请将其指出
考点:物质分离、提纯的实验方案设计,物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:由实验流程可知,试剂①为NaOH溶液,则沉淀①为Mg(0H)2,溶液①为NaCl、NaAlO2,再加盐酸,与NaAlO2反应生成AlCl3,从而实现混合物分离,以此来解答.
解答:
解:(1)若为氨水,两种金属离子均转化为沉淀,试剂①应选NaOH溶液,可使镁离子转化为沉淀,为使分离完全,该试剂的用量是过量,故答案为:NaOH溶液;过量;
(2)过滤后所得沉淀①的化学式为Mg(0H)2,沉淀①需进行洗涤,洗涤沉淀的方法是用蒸馏水浸没沉淀,重复操作几次,故答案为:Mg(0H)2;用蒸馏水浸没沉淀,重复操作几次;
(3)生成溶液①的离子方程式为Al3++4OH-=AlO2-+2H2O,故答案为:Al3++4OH-=AlO2-+2H2O;
(4)以上实验设计明显存在缺陷,氯化铝中混有NaCl,改进方法为溶液①中通入足量的二氧化碳,然后过滤,对过滤得到的固体加盐酸溶解,
故答案为:氯化铝中混有NaCl;溶液①中通入足量的二氧化碳,然后过滤,对过滤得到的固体加盐酸溶解.
(2)过滤后所得沉淀①的化学式为Mg(0H)2,沉淀①需进行洗涤,洗涤沉淀的方法是用蒸馏水浸没沉淀,重复操作几次,故答案为:Mg(0H)2;用蒸馏水浸没沉淀,重复操作几次;
(3)生成溶液①的离子方程式为Al3++4OH-=AlO2-+2H2O,故答案为:Al3++4OH-=AlO2-+2H2O;
(4)以上实验设计明显存在缺陷,氯化铝中混有NaCl,改进方法为溶液①中通入足量的二氧化碳,然后过滤,对过滤得到的固体加盐酸溶解,
故答案为:氯化铝中混有NaCl;溶液①中通入足量的二氧化碳,然后过滤,对过滤得到的固体加盐酸溶解.
点评:本题考查物质分离、提纯实验方案的设计,为高频考点,把握实验流程中的试剂、发生的反应及分离方法为解答的关键,侧重分析能力、实验能力的综合考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
实验室中制备HClO溶液的最好方法是将Cl2缓慢通入( )
| A、蒸馏水 | B、烧碱溶液 |
| C、纯碱溶液 | D、石灰石的悬浊液 |
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
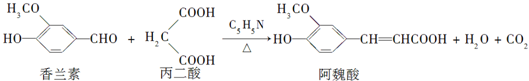
下列说法正确的是( )

下列说法正确的是( )
| A、可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
| B、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应 |
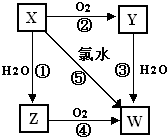 已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化
已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化
 按要求完成下列两题:
按要求完成下列两题: