题目内容
【题目】如图是实验室模拟工业生产漂白粉的装置(夹持和加热装置省略)。
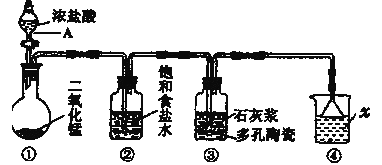
(1)写出图中仪器A的名称___;②装置中饱和食盐水的作用是___。
(2)装置①中发生反应的化学方程式为___。
(3)装置③中发生反应的化学方程式为___。
(4)装置④中发生反应的离子化学方程式为___。
【答案】分液漏斗 除去氯气中的氯化氢气体 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Cl2+2OH-= Cl-+ClO-+H2O
MnCl2+Cl2↑+2H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Cl2+2OH-= Cl-+ClO-+H2O
【解析】
利用浓盐酸和二氧化锰加热条件下反应制取氯气,发生的反应为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;由于浓盐酸具有挥发性,制取的氯气中含有氯化氢,通过②装置中的饱和食盐水除去氯化氢气体,净化后的氯气通入装置③中与石灰浆发生反应生成次氯酸钙,化学反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;氯气有毒,不能排放到大气中,未反应的氯气需要氢氧化钠溶液吸收处理,发生的反应为Cl2+2OH-= Cl-+ClO-+H2O;
MnCl2+Cl2↑+2H2O;由于浓盐酸具有挥发性,制取的氯气中含有氯化氢,通过②装置中的饱和食盐水除去氯化氢气体,净化后的氯气通入装置③中与石灰浆发生反应生成次氯酸钙,化学反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;氯气有毒,不能排放到大气中,未反应的氯气需要氢氧化钠溶液吸收处理,发生的反应为Cl2+2OH-= Cl-+ClO-+H2O;
(1)图中仪器A的名称为分液漏斗;②装置中饱和食盐水的作用是除去氯气中的氯化氢气体,
答案为:分液漏斗;除去氯气中的氯化氢气体;
(2)根据上述分析,装置①中发生反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(3)根据上述分析,装置③中发生反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(4)根据分析,装置④中发生反应的离子化学方程式为Cl2+2OH-= Cl-+ClO-+H2O,
答案为:Cl2+2OH-= Cl-+ClO-+H2O。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案