题目内容
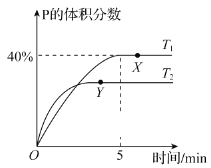
【题目】将1molM和2 molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g)![]() P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
A. 若X、Y两点的平衡常数分别为K1、K2,则K1>K2
B. 温度为T1时,N的平衡转化率为80%,平衡常数K=40
C. 无论温度为T1还是T2,当容器中气体密度和压强不变时,反应达平衡状态
D. 降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率
【答案】A
【解析】
A. 若X点P的体积分数40%,Y点P的体积分数小于40%,X点P的含量高,P为生成物,产率越大,平衡常数越大,两点的平衡常数分别为K1、K2,则K1>K2,故A正确;
B. 温度为T1时,设N的变化量为xmol,根据反应:
M(s)+2N(g)![]() P(g)+Q(g)
P(g)+Q(g)
初始(mol):1 2 0 0
变化(mol): x ![]()
![]()
平衡(mol): 2-x ![]()
![]()
温度为T1时,X点P的体积分数=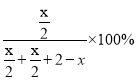 =40%,解得x=1.6mol。
=40%,解得x=1.6mol。
N的平衡转化率为=![]() =80%,平衡常数K=
=80%,平衡常数K=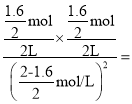 4,故B错误;
4,故B错误;
C. 该反应为反应前后气体体积不变的体系,压强不影响平衡移动,不能做为达到平衡的判断依据,故C错误;
D.该反应为反应前后气体体积不变的体系,增大压强,反应速率加快,但压强不影响平衡移动,转化率不变;根据“先拐先平数值大”的原则,T2> T1,降低温度P的体积分数减少,反应向逆向进行,即放热的方向进行,反应物的转化率较低,故D错误;
答案选A。

练习册系列答案
相关题目