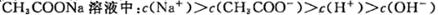题目内容
在25℃下,将a mol·L-1的CH3COONa与0.02 mol·L-1的盐酸等体积充分混合,反应后测得溶液pH=7,则:
(1)a 0.02(填“<”、“>”或“=”);
(2)c(CH3COO-)+ c(CH3COOH)= mol·L-1,c(CH3COOH)= mol·L-1;
(3)CH3COOH的电离平衡常数Ka= (用含a的代数式表达)。
(4)反应后溶液中各种离子浓度由大到小顺序是
(1)>;(2)0.5a,0.01;(3)(5a-0.1)×10-6;
(4)c(Na+)> c(CH3COO-)> c(Cl-)> c(H+)=c(OH-)(每空2分)
解析试题分析:(1)若两者刚好反应,生成氯化钠和醋酸,显酸性,要中性,醋酸钠要过量,故)a >0.02;
(2)等体积混合和,溶液体积为原来的2倍,根据物料守恒可得c(CH3COO-)+ c(CH3COOH)= 0.5a mol·L-1,根据电荷守恒:c(Na+)+ c(H+)=c(CH3COO-)+c(Cl-)+ c(OH-),已知c(Na+)=0.5a,c(Cl-)=0.01,c(H+) =c(OH-),所以c(CH3COOH)=0.01mol·L-1;(3)CH3COOH的电离平衡常数Ka= c(CH3COO-)· c(H+)/(CH3COOH)=(5a-0.1)×10-6;(4)反应后溶液中各种离子浓度由大到小顺序是c(Na+)> c(CH3COO-)> c(Cl-)> c(H+)=c(OH-)
考点:考查物料守恒、电荷守恒、离子浓度的计算。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案下表是相同温度下三种酸的一些数据,下列判断正确的是
A.在相同温度下, > > > > |
B.室温时,若在NaZ溶液中加水,则 / / · · 的比值变小,若加少量盐酸,则比值变大 的比值变小,若加少量盐酸,则比值变大 |
C.等物质的量浓度的NaX、NaY和NaZ的混合溶液,则 < < < < |
D.在相同温度,从HX的数据可以说明:弱电解质溶液浓度越低,电离度越大,且 > > > > =0.01 =0.01 |
某温度下,向一定体积0.1 mol/L的氨水中逐滴滴加0.1mol/L的盐酸,溶液中pH与pOH[注:pOH=-lgc(OH-)]的变化关系如图所示,则下列说法中错误的是
| A.M点所示溶液中c( NH4+)>c(Cl-) |
| B.Q点所示溶液的导电熊力强于M点 |
| C.Q点消耗盐酸的体积等于氨水的体积 |
| D.M点和N点所示溶液中水的电离程度相同 |
0.1 mol/L K2CO3溶液中,若要使c(CO32-)更接近0.1 mol/L,可采取的措施是
| A.加入少量盐酸 | B.加KOH固体 | C.加水 | D.加热 |
pH=2的两种一元酸X和Y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加0.1 mol/L NaOH至pH=7,消耗NaOH溶液的体积为Vx、Vy,下列说法正确的是
A.X为弱酸,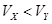 | B.Y为强酸,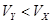 |
C.X为强酸, | D.Y为弱酸, |
常温下,往c1mo1/L的醋酸溶液中滴加同体积的c2 mo1/L的氢氧化钠溶液后,所得溶液的pH=7,则
| A.酸碱恰好中和 | B.c1=c2 |
| C.滴人酚酞溶液呈浅红色 | D.所得溶液c(Na+)=c(CH3COO一) |
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图,下列判断正确的是( )
| A.a、c两点溶液的导电能力相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc |
| D.a、b、c三点溶液水的电离程度a>b>c |
25 ℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述,正确的是 ( )。
| A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32—)+c(OH-)+c(Cl-) |
| B.pH=4的溶液中:c(H2CO3)+c(HCO3—)+c(CO32—)<0.1 mol·L-1 |
| C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3—)=c(OH-)+c(Cl-) |
| D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32—)>c(HCO3—)>c(H2CO3) |
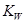 随着温度的升高而增大,说明水的电离是放热反应
随着温度的升高而增大,说明水的电离是放热反应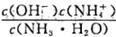 增大
增大