题目内容
下列叙述正确的是
A.两种难溶物质比较,溶度积小的溶解度不一定小
B.水的离子积常数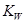 随着温度的升高而增大,说明水的电离是放热反应
随着温度的升高而增大,说明水的电离是放热反应
C.向0.1mol/L的氨水中加入少量硫硫酸固体,则溶液中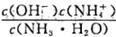 增大
增大
D:0.1mol/L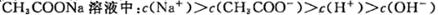
A
解析试题分析:A、组成和结构两种难溶物质比较,溶度积小的溶解度一定小,组成和结构不相似的难溶物不能通过溶度积直接比较溶解度大小,正确;B、水的离子积常数KW随着温度的升高而增大,说明水的电离是吸热反应,错误;C、题给表达式为一水合氨的电离常数表达式,电离常数的影响因素为温度,向0.1mol/L的氨水中加入少量硫酸铵固体,电离常数不变,错误;D、醋酸钠为强碱弱酸盐,水解显碱性,c(H+)<c(OH—),错误。
考点:考查电解质溶液,涉及沉淀溶解平衡、弱电解质的电离及盐类的水解应用。

练习册系列答案
相关题目
升高温度,0.01 mol·L-1下列溶液的pH基本不变的是
| A.NaOH | B.H2SO4 | C.NaCl | D.Na2CO3 |
常温时,下列叙述正确的是 ( )
| A.稀释pH=3的醋酸,溶液中所有离子的浓度均降低 |
B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,则混合液中 |
| C.pH均为11的NaOH和Na2CO3溶液中,水的电离程度相同 |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
水是一种极弱的电解质,在室温下,KW=1×10-14,则此时水的电离百分数为:
| A.1×10-7 | B.1/55.6 | C.10-14 | D.1/(55.6×107) |
下列比较中,正确的是
| A.同温和同物质的量浓度时,HF比HCN易电离,则溶液pH:NaF>NaCN |
| B.物质的量浓度相等的H2S和NaHS混合溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C.0.1mol/L的醋酸溶液加水稀释,c(H+)、c(OH-)同比例减小 |
| D.体积相同、pH相同的NH4Cl溶液、盐酸,完全溶解少量且等量的锌粉,前者用时长 |
化学平衡常数(K)、弱酸的电离平衡常数(Ka)、难溶物的溶度积常数(Ksp)是判断物质性质或变化的重要的平衡常数。下列关于这些常数的说法中,正确的是( )
| A.平衡常数的大小与温度、浓度、压强、催化剂等有关 |
| B.当温度升高时,弱酸的电离平衡常数Ka变小 |
| C.Ksp(AgCl)>Ksp(AgI),由此可以判断AgCl(s)+I-(aq)=AgI(s)+Cl-(aq)能够发生 |
| D.Ka(HCN)<Ka(CH3COOH),说明物质的量浓度相同时,氢氰酸的酸性比醋酸强 |
用水稀释0.1 mol·L-1氨水时,溶液中随水量的增加而减小的是( )。
| A.c(OH-)/c(NH3·H2O) |
| B.c(NH3·H2O)/c(OH-) |
| C.n(OH-)和c(H+) |
| D.c(H+)和c(OH-)的乘积 |
室温时,1 L 0.15 mol·L-1的NaOH溶液充分吸收2.24 L CO2(标准状况),然后温度恢复到室温。下列有关反应后溶液的判断正确的是 ( )。
| A.pH<7 |
| B.溶质为NaHCO3 |
| C.2c(Na+)=3[c(H2CO3)+c(HCO3—)+c(CO32—)] |
| D.c(Na+)>c(CO32—)>c(HCO3—)>c(OH-)>c(H+) |