题目内容
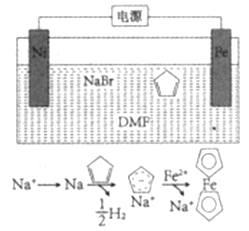
【题目】工业上电解 Na2CO3的原理如图所示。下列说法不正确的是( )

A. 阴极产生的物质 A 是 H2
B. 电解一段时间后,阳极附近溶液的 PH 将增大
C. 该离子交换膜应为阳离子交换膜
D. 阳极电极反应为 4CO32-+2H2O-4e-=4HCO3-+O2↑
【答案】B
【解析】
工业上电解 Na2CO3溶液,根据装置图分析,电解池阳极发生的反应为物质失去电子,发生氧化反应,碳酸钠转化为碳酸氢钠,则阳极电极反应为:4CO32-+2H2O-4e-=4HCO3-+O2↑,阴极为物质得到电子,发生还原反应,生成氢氧化钠,则阴极反应式为:2H2O+2e-═2OH-+H2↑,据此分析判断。
A. 阴极发生还原反应,反应式为:2H2O+2e-═2OH-+H2↑,则阴极产生的物质A是H2,故A正确;
B. 阳极电极反应为:4CO32-+2H2O-4e-=4HCO3-+O2↑,溶液的碱性减弱,所以电解一段时间后,阳极附近溶液的 pH 将减小,故B错误;
C. 由于阴极产品为氢氧化钠,阳极区的钠离子要进入阴极区,所以离子交换膜应为阳离子交换膜,故C正确;
D. 阳极发生氧化反应,阳极电极反应为 4CO32-+2H2O-4e-=4HCO3-+O2↑,故D正确。
故选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目