题目内容
【题目】下列氧化还原反应中,电子转移的方向和数目均正确的是( )
A.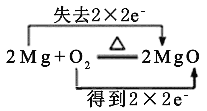
B.
C.
D.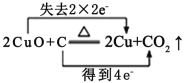
【答案】A
【解析】
A. Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4;
B.反应中Cl元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为12;
C. 氧化还原反应中得失电子数应该相等;
D. CuO与C反应中,铜得电子,C失电子。
A. Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4,则电子转移的方向和数目为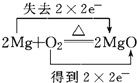 ,A项正确;
,A项正确;
B. 该反应中Cl元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为12,则电子转移的方向和数目为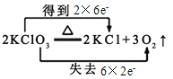 ,B项错误;
,B项错误;
C. 氧化还原反应中得失电子数应该相等,则碳与氧气反应时,电子转移的方向和数目为 ,C项错误;
,C项错误;
D. CuO与C反应,铜得电子,C失电子,则电子转移的方向和数目为 ,D项错误;
,D项错误;
答案选A。

练习册系列答案
相关题目
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
K为化学平衡常数,其中K和温度的关系如下表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是
A. 此反应为放热反应
B. 此反应只有达到平衡时,密闭容器中的压强才不会变化
C. 此反应达到1 000℃时的反应速率比700℃时大
D. 该反应的化学平衡常数越大,反应物的转化率越低

