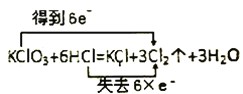
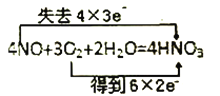
题目内容
【题目】下列关于难溶电解质溶解平衡的说法正确的是
A. 可直接根据 Ksp 的数值大小比较难溶电解质在水中的溶解度大小
B. 在 AgCl 的饱和溶液中,加入蒸馏水, Ksp(AgCl)不变
C. 难溶电解质的溶解平衡过程是可逆的,且在平衡状态时 v溶解=v沉淀=0
D. 25℃时, Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量 KI 固体,一定有黄色沉
【答案】B
【解析】
A、比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,比较同类型的难溶物的溶解度大小,可通过溶度积直接比较溶解度大小,故A错误;
B、在纯水中物质的溶解度和Ksp都只受物质性质和温度的影响,与其它外界条件无关,所以B选项是正确的;
C、平衡状态时v溶解=v沉淀![]() 0,电解质的溶解和离子结晶形成电解质都在继续,故C错误;
0,电解质的溶解和离子结晶形成电解质都在继续,故C错误;
D、加入KI后碘离子浓度增大,使得碘离子浓度与银离子浓度之积增大,可能会大于Ksp(AgI),若加入足量的碘化钾,则有黄色沉淀碘化银生成,但不一定,故D错误。
所以B选项是正确的。

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案【题目】硫代硫酸钠晶体(![]() ,
,![]() )可用作还原剂。回答下列问题:
)可用作还原剂。回答下列问题:
(1)已知:![]() ,
,![]() 都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀![]() 、
、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液
溶液
实验步骤 | 现象 |
①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
③取少量溶液溶于盐酸 | ④出现乳黄色浑浊,_____ |
⑤静置,________ | ⑥_______ |
(2)利用![]() 作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制;称取1.270g纯净的![]() ,在盛有KI溶液的____(填仪器名称,下同)中溶解(反应为
,在盛有KI溶液的____(填仪器名称,下同)中溶解(反应为![]() ,
,![]() 能够充分反应),完全溶解后,全部转移至100 mL的____中,加蒸馏水至刻度线,此时
能够充分反应),完全溶解后,全部转移至100 mL的____中,加蒸馏水至刻度线,此时![]() 溶液的物质的量浓度为____
溶液的物质的量浓度为____![]() ;再取
;再取![]() 样品配制成溶液,备用。
样品配制成溶液,备用。
②滴定:利用发生反应:![]() ,对上述配制的
,对上述配制的![]() 溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为___%(保留1位小数。
溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为___%(保留1位小数。
【题目】一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的下列 3 种溶液的 pH:
溶质 | NaHCO3 | Na2CO3 | NaClO |
pH | 8.34 | 11.6 | 10.3 |
下列有关说法正确的是( )
A. 以上溶液的 pH 是用广泛 pH 试纸测定的
B. 反应CO2+H2O+2NaClO=Na2CO3+2HClO可以发生
C. 室温下,电离常数: K2( H2CO3)>K( HClO)
D. 在新制氯水中加入少量 NaHCO3固体可以提高溶液中 HClO 的浓度
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成C; ③比例模型为: |
B | ①由C、H两种元素组成; ②球棍模型为: |
C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③与二甲醚互为同分异构体。 |
D | ①相对分子质量比C物质少2; ②能由物质C氧化而成。 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为___________(系统命名法);写出该生成物与足量的NaOH水溶液共热的化学方程式___________。
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=________时,这类有机物开始出现同分异构体。
(3)B具有的性质是________(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤高锰酸钾酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式为: _______
(4)写出由C氧化生成D的化学方程式________。