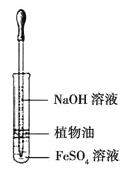
��Ŀ����
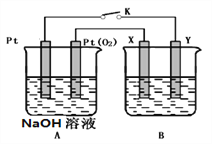
����Ŀ�����Ȼ�������ɫҺ�壬�е�Ϊ136�棬����ˮ�⡣��800���£�������ͨ���������Ѻ�̿�۵Ļ������Ƶ����Ȼ��ѣ�ͬʱ����һ���ж����塣װ������ͼ��
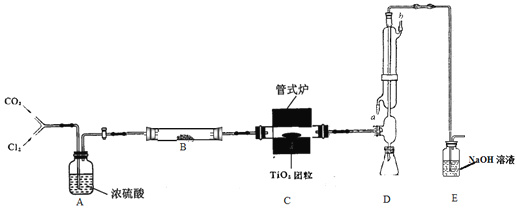
��1��ʵ�鲽�裺
�Ƚ�����TiO2��̿�ۻ�Ͼ��ȣ��Ƴɶ��״TiO2������Ȼ��������²�������ȷ��˳��Ϊ____________________������ţ���
��ͨ��CO2���岢��ʼ���ȣ�
�ڹ۲췴Ӧ�ѻ�����ɣ�ֹͣ���ȣ���ͨCO2����ֱ����ȴ�����£�
�۽�TiO2��������ɹ����ʵ�λ�ã������Ӻ�����װ�ã�
�ܵ���ʽ¯���µ�800����ͨCl2��ͬʱ����������ͨ����ˮ��
��ȡ����ƿ������������������
ʵ���в�ֱ��ʹ�ö������Ѻ�̿�ۣ��������Ƴɶ��״TiO2������ԭ����_________��
��2������������ˮ�����Ϊ________�����ţ���
��3��װ��B��װ��ҩƷΪ_____________������Ϊ________________��ʵ��������ͨ��CO2�����еڶ���ͨ��CO2��������______________������_______�������CO2������һ�֣���
��4�����ϲ���ڣ��۲쵽��������________________ʱ����ȷ����Ӧ�ѻ�����ɡ�
��5���Ʊ���Ӧ����Ҫ��ѧ����ʽΪ_________________________________________��
��6����װ�ô������Ե�ȱ�ݣ�����Ľ���ʩ__________________________________��
���𰸡� �ۢ٢ܢڢ� ����Ӧ��Ӵ��� a ��ˮ����ͭ ����װ���е�ˮ�����Ƿ���� �����ɵ�TiCl4������ȫ���������ܣ���ֹ��ȴʱ���ռ���Һ��ˮ������������ƿ�� N2 ������ĩ��û��TiCl4Һ�μ������� TiO2��2C��2Cl2![]() TiCl4��2CO ��װ��ĩ�ˣ���ڴ�����һյ��ȼ�ľƾ���
TiCl4��2CO ��װ��ĩ�ˣ���ڴ�����һյ��ȼ�ľƾ���
��������������������һ�������Ʊ���ʵ����������ʱ��Ӧ���ȷ�����Ŀ�и�����Ҫ�Ʊ������ʵĻ����������ٸ���װ��ͼ���ֳ�ÿ��װ�õ����������н����
��⣺��1��ʵ����Ӧ��������װ�ü���ҩƷ��ͨ�������̼�ų�װ�õĿ�������ͨ���������з�Ӧ��Ȼ���ڶ�����̼��������ȴ������������ӣ���ֹˮ�⡣����˳��Ϊ���ۢ٢ܢڢݡ��Ƚ�����TiO2��̿�ۻ�Ͼ��ȣ��Ƴɶ��״TiO2������������������Ӧ��ĽӴ�������ӿ췴Ӧ������
��2������ˮӦ���¿����Ͽڳ����������Ϊa��
��3��װ��B��Ӧ�ü�����ˮ����ͭ����֤ˮ����������ȥ��ʵ���������ͨ�������̼��Ŀ����Ϊ��ʹ�������ڶ�����̼��������ȴ��ͬʱҲ��������װ���в�����TiCl4����D�У�Ҳ�ܷ�ֹ����������Һ��ˮ����������D�С�ʵ���п���ʹ������Ķ���������������̼�����磺������ϡ�����塣
��4�����ϲ�����������Ӧ������ʱ����û��TiCl4������������D���������¶˾Ͳ�������Һ�ε��¡�
��5���Ʊ���Ӧ�Ƕ������ѡ�̼�ۡ�������Ӧ�õ�TiCl4���ж����壨CO�������Է�ӦΪ��TiO2��2C��2Cl2![]() TiCl4��2CO��
TiCl4��2CO��
��6����װ�ô������Ե�ȱ�������ɵ�COû�н���β�����������ԸĽ���ʩΪ����װ��ĩ�ˣ���ڴ�����һյ��ȼ�ľƾ�������COȼ��Ϊ������̼��

����Ŀ�����ú�ͭ�����Ĵ�п�Ʊ�����п��������ʡ���������ͼ���й��������£�

���� | Cu(OH)2 | Zn(OH)2 | Fe(OH)3 | ZnS | CuS |
Ksp | 5.0��10��20 | 2.0��10��16 | 4.0��10��38 | 1.2��10��23 | 8.5��10��45 |
��ش��������⣺
��1����п�е�ͭ������ϡ��Һ��Ӧ�Ļ�ѧ����ʽΪ__________________________��ͼ�д�������XҪ�ܹ�������ɫ��ѧ˼�룬���貹������______���ѧʽ����
��2������ҺI��c(Cu2��)Ϊ0.05mol��L��1������ҺII��c(Fe3��)��____mol��L��1��
��3��������A��Zn��ȡ9.61 g����C�ܽ���������500mL 2 mol��L��1ϡ�����У����ռ�����״����2.24L�����壬��������Һ�м���2 mol��L��1NaOH��Һ�������ɳ������ʱ������������Ϊ_____g��������A����һ�����ʣ�ȡ���ֹ���C���Թ��У�������������г�����ζ���壬��÷�Ӧ�����ӷ���ʽΪ________________________��
��4����Һ������Ũ����____________�����ˡ�ϴ�ӡ�������õ��ϴ���������п���壻��Һ�������Ʊ�ZnS��ʵ��ѡ����ǣ�NH4��2S��Һ������Na2S��Һ��Ϊ��Ӧ������Ǻ����Ƶõ�ZnS���н϶�����ʣ����������____________���ѧʽ����
��5������п���������Ըɵ�صĸ������ɵ�ز�ʹ��ʱ�����ڸ�����������Һ�Ӵ��������Էŵ練Ӧ��2NH4����Zn��2NH3��H2����Zn2������ɵ����Զ����١�д��Ǧ���ز�ʹ��ʱ���������Ϸ����Էŵ�Ļ�ѧ����ʽ__________________________��
����Ŀ��ijѧϰС���о�NaOH��ijЩ��֮��ķ�Ӧ��
���к��ȵIJⶨ
��25�桢101kPa�����£�ǿ����ǿ���ϡ��Һ�к��ȿɱ�ʾΪ��H+(aq)+OH��(aq)=H2O(l) ��H=-57.3kJ ��mol��1������ͼ1��ʾװ�ý���ʵ�顣
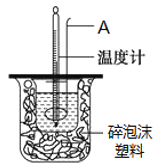
��1������A��������________��
��2������ĭ���ϵ�������________��
��3����25�桢101kPa�����£�ȡ50mL 0.50 mol��L��1 CH3COOH��Һ��50mL 0.55 mol��L��1 NaOH��Һ����ʵ�飬��õ��к��ȡ�H________-57. 3 kJ ��mol��1���������=����������ԭ���� ________��
���к͵ζ�
��1����_______��ȡ20.00 mL����ϡ������Һ������ƿ�У����μ�1��2�η�̪��ָʾ������0.20 mol��L��1NaOH����Һ���еζ���Ϊ�˼�Сʵ������ͬѧһ������������ʵ�飬����ÿ����ȡϡ���������Ϊ20.00 mL������ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
����NaOH��Һ���/mL | 19.00 | 23.00 | 23.02 |
�������Ũ��ԼΪ________ (������λ��Ч����)���ζ��ﵽ�յ�ı�־��________��
��2����ij�εζ�����ʱ���ζ���Һ����ͼ2��ʾ�����յ����Ϊ________mL��