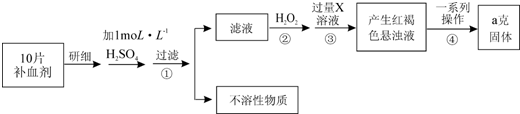
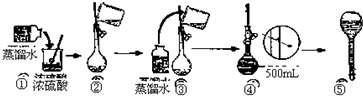
题目内容
19.在两支分别盛有Al(OH)3的试管中,向其中一支中滴加足量盐酸,观察到的现象是沉淀溶解,发生反应的离子方程式为Al(OH)3+3H+═Al3++3H2O;向另一支滴加足量NaOH溶液,观察到的现象是沉淀溶解,发生反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.由此说明Al(OH)3是一种两性氢氧化物.分析 Al(OH)3为两性氢氧化物,可与酸反应生成Al3+,与碱反应生成AlO2-,以此解答该题.
解答 解:在两支分别盛有Al(OH)3的试管中,向一份中加入过量的稀硫酸,氢氧化铝与硫酸反应生成硫酸铝铝与水,沉淀溶解反应离子方程式为:Al(OH)3+3H+═Al3++3H2O,向另一份中加入过量的氢氧化钠溶液,氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,沉淀溶解,反应离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,说明氢氧化铝是两性氢氧化物,
故答案为:沉淀溶解;Al(OH)3+3H+═Al3++3H2O;沉淀溶解;Al(OH)3+OH-═AlO2-+2H2O;两性.
点评 本题考查氢氧化铝的性质、离子方程式书写等,为高频考点,但题目比较基础,注意对基础知识的理解掌握,难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
9.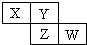 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | 原子半径:X<Z<W | |
| B. | 气态氢化物的稳定性:X>Y | |
| C. | 非金属性:Z>Y | |
| D. | 最高价氧化物对应水化物的酸性:W>Z |
10.如图所示,电极a和b均为石墨棒,在电解过程中,下列说法正确的是( )
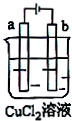

| A. | 电极a表面呈红色 | |
| B. | 电极b作阳极 | |
| C. | 电子由电源的正极沿导线流向电极a | |
| D. | 该装置能量转化形式为电能转化为化学能 |
11.等质量的下列物质分别完全燃烧,生成CO2的量最多的是( )
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | C2H6O |
8.能正确表示下列反应的离子方程式是( )
| A. | Cl2与水的反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | H2SO4与Ba(OH)2反应:Ba2++SO42-═BaSO4 | |
| C. | 铁溶于足量的稀硝酸:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 碳酸氢钙溶液跟足量烧碱溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
2.某小组探究Na2CO3和NaHCO3的性质,实验步骤及记录如下:
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入过量的10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.得到表1的数据:
表1
回答下列问题:
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为还应该增加一个实验,并补做如下实验:10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
D.利用上述实验数据即可计算:CO32-(aq)+2H+(aq)=H2O(l)+CO2(g)的△H
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84({m}_{1}-{m}_{2})}{31{m}_{1}}×100%$(用代数式表示).
附表:溶解度表
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入过量的10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.得到表1的数据:
表1
| 温度 试剂 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为还应该增加一个实验,并补做如下实验:10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
D.利用上述实验数据即可计算:CO32-(aq)+2H+(aq)=H2O(l)+CO2(g)的△H
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84({m}_{1}-{m}_{2})}{31{m}_{1}}×100%$(用代数式表示).
附表:溶解度表
| 溶解度 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |