题目内容
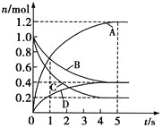
【题目】一定温度下,向容积为![]() 的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是
的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是
A.该反应的化学方程式为6A+2D![]() 3B+4C
3B+4C
B.反应进行到![]() 时,
时,![]()
C.反应进行到![]() 时,B的平均反应速率为0.12mol/(L.min)
时,B的平均反应速率为0.12mol/(L.min)
D.反应从![]() 到4s时,C的反应速率逐渐减小
到4s时,C的反应速率逐渐减小
【答案】D
【解析】
由图可知,平衡前,B、C的物质的量随着反应的进行而减小,A、D的物质的量随着反应的进行而增大,所以,B、C是反应物,A、D是生成物。平衡前,A、B、C、D四种物质的变化量之比=1.2:(1.0-0.4):(1.0-0.2):0.4=6:3:4:2,则该反应的方程式为:3B+4C![]() 6A+2D,据此解答。
6A+2D,据此解答。
A.该反应的化学方程式为:3B+4C![]() 6A+2D,A错误;
6A+2D,A错误;
B.由方程式可知,![]() ,B错误;
,B错误;
C.前5s,v(B)=![]() =0.06mol/(L·s),C错误;
=0.06mol/(L·s),C错误;
D.反应从![]() 到4s,C的浓度减小,反应速率逐渐减小,D正确。
到4s,C的浓度减小,反应速率逐渐减小,D正确。
答案选D。

【题目】300℃时,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g) +Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
回答下列问题:
(1)反应0~2 min Z的平均速率v(Z)=_____________
(2)能判断该反应已经达到平衡状态的是_____________
A.生成X的速率是生成Z的速率的2倍
B.容器内压强保持不变
C.容器内气体的密度保持不变
D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是_____________(任写一种)。
(4)温度为300℃时,该反应的化学平衡常数K=_______________
(5)若起始时向该容器中充入X、Y、Z各0.20 mol,则反应将向____(填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比______(填“增大”、“减小”或“不变”)