题目内容
14.下列各组元素中,按最高正价递增的顺序排列的是( )| A. | N、O、F | B. | Li、Al、Mg | C. | Li、B、C | D. | Cl、Br、I |
分析 元素的最高正价=最外层电子数,同主族元素最高正化合价相等,注意氧元素没有最高正价,氟元素无正价,据此分析.
解答 解;A.N、O、F最外层电子数依次为5、6、7,而O、F元素没有最高正化合价,故A错误;
B.Li、Al、Mg最外层电子数依次为1、3、2,其最高化合价分别为+1、+3,+2,故B错误;
C.Li、B、C最外层电子数依次为1、3、4,其最高化合价分别为+1、+3,+4,按最高正价递增的顺序排列,故C正确;
D.Cl、Br、I位于同一主族,最外层电子数均为7,其最高化合价均为+7,故D错误.
故选C.
点评 本题考查原子结构与性质关系,难度不大,注意主族元素最高正化合价=最外层电子数=主族族序数,但氧、氟元素没有最高正价

练习册系列答案
相关题目
4.某气态烃1mol能与2mol HCl完全加成,加成后产物分子中的氢原子又可被6mol Cl2完全取代,则此气态烃可能是( )
| A. | CH3C≡CCH3 | B. | CH2=CH2 | C. | CH≡CCH3 | D. | CH2=CHCH3 |
5.下列有关化学用语使用正确的是( )
| A. | 硫原子的原子结构示意图: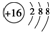 | |
| B. | 氚原子可表示为${\;}_{1}^{2}$H | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | 铁位于周期表第4周期第ⅧB族 |
2.2014年6月5日为世界环境日,主题为“提高你的呼声而不是海平面”,提倡节能减排,以下措施中不能体现这一思想的是( )
| A. | 提倡绿色生活,使用公共交通 | |
| B. | 大力发展火电,缓解用电紧张 | |
| C. | 开发太阳能、风能、氢能等清洁能源 | |
| D. | 研制出性能优良的催化剂,降低反应所需温度 |
9.工业上铁的冶炼是在炼铁高炉中进行的,发生的反应是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,对于该反应,下列说法正确的是( )
| A. | 反应中转移3个电子 | B. | Fe2O3发生还原反应 | ||
| C. | CO被还原 | D. | CO为氧化剂 |
19.下列过程中化学键未被破坏的是( )
| A. | 碘升华 | B. | 溴与H2生成HBr | C. | SO2气体溶于水 | D. | NaCl固体溶于水 |
6.某短周期元素的L层电子数是K层电子数的3倍,该元素的符号为( )
| A. | C | B. | S | C. | O | D. | Si |
3.原子序数为x的元素位于周期表中的第ⅡA族,则原子序数为x+1的元素不可能为( )
| A. | 第ⅢA族 | B. | 第ⅠA族 | C. | 镧系元素 | D. | 第ⅢB族 |
4.已知KMnO4、浓盐酸在常温下反应能生成Cl2.若用如图所示的实验装置来制备纯净、干燥的氯气,并实验它与金属的反应.每个虚线框表示一个单元装置,其中有错误的是( )
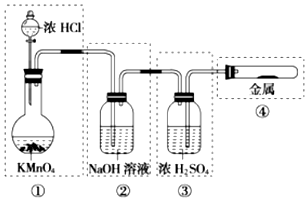

| A. | ①和②处 | B. | ②处 | C. | ②和③处 | D. | ②③④处 |