题目内容
14. 金属铝、铁、铜及其化合物与生产、科研关系密切.
金属铝、铁、铜及其化合物与生产、科研关系密切.(1)工业上可用铝与软锰矿(主要成分为MnO2)反应冶炼金属锰.用化学方程式表示其冶炼原理3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3.
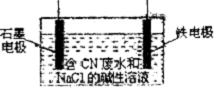
(2)工业上,采用石墨、铁棒作为电极,电解除去废水中的CN-(C为+4价.下同),装置如图所示,通电过程中,阴、阳两极均有无色无味的气体产生,阳极区两种离子的放电产物会进一步发生反应,其方程式为C12+CNO-+OH-→□+Cl-+CO32-+H2O(未配平).
①铁电极应连接直流电源的负极(填写电极名称).
②上述反应方程式配平后“□”内应填写N2.
③阴极产物有氢气,阳极上发生的电极反应为2Cl--2e-=Cl2↑和CN--2e-+2OH-═CNO-+H2O.
(3)用 CuSO4溶液为电解质溶液,进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼.下列说法错误的是ac(填写字母代号).
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(4)硫酸铝铵水溶液呈酸性,是因为Al3+、NH4+(填写离子符号)发生了水解;常温下浓度均为0.1mol•L-1硫酸铝和硫酸铝铵两种水溶液,c(Al3+)较大的是硫酸铝铵(填“硫酸铝铵”或“硫酸铝”)溶液.
分析 (1)高温时,铝与二氧化锰发生置换反应生成锰,为铝热反应;
(2)根据发生的电极反应,可以知道金属铁是阴极,石墨电极是阳极,根据电解质中离子的放电顺序以及电极反应和电子的转移知识来回答即可;
(3)电解精炼铜时,粗铜作阳极,该电极上Zn、Fe、Ni、Cu失电子,精铜作阴极,该极上是铜离子得电子,阳极上铜以及比铜活泼的金属会溶解,而没有铜活泼的金属会从阳极掉落下,形成阳极泥;
(4)铝离子、铵离子水解使溶液显示酸性;根据铵离子水解使溶液显示酸性,硫酸铝铵溶液中氢离子浓度大于硫酸铝溶液的,氢离子抑制了铝离子的水解.
解答 解:(1)高温时,铝与二氧化锰发生置换反应生成锰,反应的方程式为3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3,
故答案为:3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3;
(2)①根据发生的电极反应,可以知道金属铁是阴极,接电源的负极,故答案为:负极;
②据氧化还原反应的原理,其反应方程式为3Cl2+2CNO-+8OH-═N2+6Cl-+2CO32-+4H2O,故答案为:N2;
③阴极上氢离子放电发生还原反应,生成氢气,阳极发生氧化反应,阳极的电极反应式为:CN--2e-+2OH-═CNO-+H2O和2Cl--2e-═Cl2↑,
故答案为:氢气;CN--2e-+2OH-═CNO-+H2O;
(3)a、电解池中,电能不会全部转化为化学能,还会伴随热能等形式的能的产生,故a错误;
b、电解精炼铜时,粗铜作阳极,接电源正极,发生氧化反应,故b正确;
c、溶液中Cu2+向阴极移动,在阴极上发生还原反应,故c错误;
d、在阳极上,没有铜活泼的金属Ag、Pt、Au等金属会从阳极掉落下,形成阳极泥,利用阳极泥可回收Ag、Pt、Au等金属,故d正确;
故答案为:ac;
(4)在硫酸铝铵溶液中,铝离子、铵离子水解,使溶液显示酸性,反应的离子方程式为:Al3+﹢3H2O?Al (OH)3﹢3H+; NH4++H2O?NH3•H2O+H+;根据铵离子水解使溶液显示酸性,硫酸铝铵溶液中氢离子浓度大于硫酸铝溶液的,氢离子抑制了铝离子的水解,况且浓度均为0.1mol•L-1硫酸铝和硫酸铝铵两种水溶液中,铝离子浓度分别为0.2mol/L和0.1mol/L,所以硫酸铝铵溶液中铝离子浓度较大;
故答案为:Al3+、NH4+; 硫酸铝铵.
点评 本题考查了铝热反应、电解原理及其应用、盐类水解,注意知识的归纳和整理以及应用是关键,难度不大.

| A. | 通CO的一极是电池的正极 | |
| B. | 该电池工作过程中需不断补充CO和O2,CO2可循环利用 | |
| C. | 负极反应式为:O2+2CO2+4e-→2CO32- | |
| D. | 正极反应式为:2CO+2CO32-→4CO2+4e- |
①CO(g)+2H2(g)?CH3OH(g)△H1=-Q1 kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-Q2 kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-Q3 kJ•mol-1
回答下列问题:
(1)新工艺的总反应3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-(2Q1+Q2+Q3)kJ/mol.
(2)工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH (g)△H.下表所列数据是该反应在不同温度下的化学平衡常数(Κ).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
A.体系的压强不变
B.密度不变
C.混合气体的相对分子质量不变
D.c(CO)=c(CH3OH)
②某温度下,将 2mol CO和 6mol H2 充入2L的密闭容器中,充分反应 10min后,达到平衡时测得c(CO)=0.2mol/L,计算此温度下的平衡常数K=2.04.
(3)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨.合成氨反应原理为:N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g)△H=-92.4kJ•mol-1.实验室模拟化工生产,在恒容密闭容器中充入一定量N2和H2后,分别在不同实验条件下反应,N2浓度随时间变化如图1.请回答下列问题:
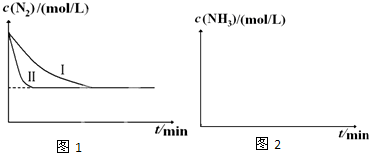
①与实验Ⅰ比较,实验Ⅱ改变的条件为加入催化剂.
②在实验Ⅲ中改变条件为采用比实验Ⅰ更高的温度,请在图2中画出实验Ⅰ和实验Ⅲ中c(NH3)随时间变化的示意图.
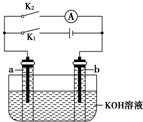 如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )| A. | 断开K2,闭合K1一段时间,溶液的pH变大 | |
| B. | 断开K1,闭合K2时,b极上的电极反应式为:2H++2e-═H2↑ | |
| C. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O | |
| D. | 断开K1,闭合K2时,OH-向b极移动 |
| A. | HNO3溶液 | B. | NaOH溶液 | C. | H2SO4溶液 | D. | 盐酸 |
| A. | 氧气通入氢硫酸 | B. | H2S缓慢通入饱和氯水 | ||
| C. | H2S缓慢通入亚硫酸 | D. | SO2缓慢通入氢硫酸 |

下表为t℃时,有关物质的pKp(注:pKp=-1gKp)
| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKp | 37.4 | 19.3 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
②滤液1的pH>(填“>”“<”或“═”)MnSO4浸出液的pH.
③加入MnF2的目的除去Ca2+(填“Ca2+”、“Fe3+”、或“Cu2+”)
 密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡状态,经测定增大压强p时,A的转化率随p而变化的曲线如图所示:
密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡状态,经测定增大压强p时,A的转化率随p而变化的曲线如图所示: