题目内容
9.将5.4g Al投入200.0mL 2.0mol•L-1的某溶液中有H2产生,充分反应后有金属剩余.该溶液可能为( )| A. | HNO3溶液 | B. | NaOH溶液 | C. | H2SO4溶液 | D. | 盐酸 |
分析 200.0mL 2.0mol•L-1的某溶液中溶质的物质的量为0.2L×2.0mol•L-1=0.4mol,Al的物质的量为$\frac{5.4g}{27g/mol}$=0.2mol,利用反应判断金属过量,并生成氢气即可.
解答 解:200.0mL 2.0mol•L-1的某溶液中溶质的物质的量为0.2L×2.0mol•L-1=0.4mol,Al的物质的量为$\frac{5.4g}{27g/mol}$=0.2mol,
A、因Al与HNO3溶液不生成氢气,则不符合题意,故A错误;
B、由2Al+2OH-+2H2O═2AlO2-+3H2↑,0.2molAl与0.4molNaOH溶液溶液反应时,碱过量,故B错误;
C、由2Al+6H+═2Al3++3H2↑,0.2molAl与0.4molH2SO4溶液,硫酸过量,故C错误;
D、由2Al+6H+═2Al3++3H2↑,0.2molAl与0.4molHCl溶液,Al过量,故D正确;
故选D.
点评 本题考查铝的化学性质,明确铝与酸碱发生的化学反应是解答的关键,并注意利用量来判断过量问题即可解答.

练习册系列答案
相关题目
19.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M2、W2Z2均为共价化合物 | |
| C. | 由X元素形成的单质不一定是原子晶体 | |
| D. | 由Y、Z、M三种元素形成的化合物一定只有共价键 |
1.25℃时,将pH=2的CH3COOH溶液和pH=12的NaOH溶液等体积混合后溶液pH=a,以下关于所得溶液的关系式肯定错误的是( )
| A. | a>7 | B. | c(CH3COOH)-c(OH-)>10-amol/L | ||
| C. | c(Na+)=c(CH3COOH)+c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
18.在下列影响化学反应速率因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末.
| A. | 只有①②③ | B. | 只有①②④ | C. | 只有③④ | D. | ①②③④ |
3.已知浓硫酸与木炭粉在加热条件下的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑十CO2↑2H2O↑.酸性KMnO4溶液可以吸收SO2,试用如图所示各装置设计一个实验,验证上述反应所产生的各种产物.
(1)这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):④→②→①→③.
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
| 编号 | ① | ② | ③ | ④ |
| 装置 | 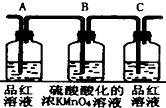 | 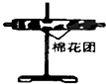 |  | 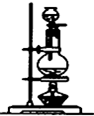 |
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.

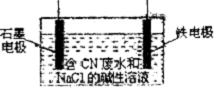 金属铝、铁、铜及其化合物与生产、科研关系密切.
金属铝、铁、铜及其化合物与生产、科研关系密切.