题目内容
1.25℃时某气态烃与O2混合充入密闭容器中,点燃后又恢复至25℃,此时容器内压强为原来的$\frac{1}{3}$,再经NaOH溶液处理,容器内几乎成为真空,该烃的化学时为( )| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
分析 经氢氧化钠溶液处理后,容器内几乎变为真空,说明气态烃和氧气完全反应,设该烃的分子式为CxHy,点燃爆炸后,又恢复到起始温度,此时容器内的压强减至原压强的$\frac{1}{3}$,剩余气体为CO2,生成的二氧化碳的分子物质的量是烃与氧气总物质的量的$\frac{1}{3}$,根据燃烧的通式进行计算.
解答 解:烃燃烧后的气体经NaOH溶液吸收,容器几乎成真空,说明烃和O2完全反应生成CO2和液态水,
设此碳氢化合物的化学式为CxHy,则:
4CxHy+(4x+y)O2$\stackrel{点燃}{→}$4xCO2+2yH2O(l)
根据题意可知:4+4x+y=3×4x,
整理可得:8x=4+y,即
若x=1,则y=4,为甲烷(CH4),
若x=2,则y=12,不存在该物质,
若x=3,则y=20,不存在该物质,
根据分析可知,该气态烃只能为甲烷,即A符合,
故选A.
点评 本题考查有机物分子式的确定,题目难度中等,明确反应前后压强的变化是解答该题的关键,易错点为根据燃烧的进行计算,注意认真体会.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.将1mol甲烷和适量的Cl2混合后光照,充分反应后生成CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为( )
| A. | 1.5mol | B. | 3mol | C. | 4.5mol | D. | 6mol |
13.关于化合物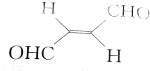 ,下列叙述正确的有( )
,下列叙述正确的有( )
 ,下列叙述正确的有( )
,下列叙述正确的有( )| A. | 分子间可形成氢键 | B. | 分子中既有极性键又有非极性键 | ||
| C. | 分子中有7个σ键和1个π键 | D. | C原子的杂化方式是sp2和sp3 |
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.
