��Ŀ����
����Ŀ��H2S��SO2��Ի��������彡�����������Σ������ҵ�ϲ�ȡ���ַ���������Щ�к�������ŷţ��ش����и������е����⡣
��H2S�ij�ȥ
����1��������H2S��ԭ��Ϊ��
H2S+Fe2(SO4)3![]() S��+2FeSO4+H2SO4
S��+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
��1����˾�����ʱ��FeSO4����������������ʱ��5��105�����þ���������______________��
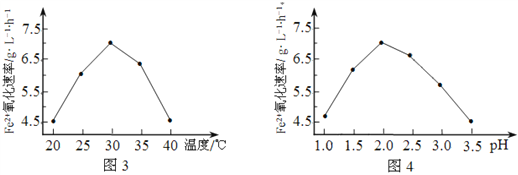
��2����ͼ3��ͼ4�ж�ʹ����˾����������Ϊ______________������Ӧ�¶ȹ��ߣ���Ӧ�����½�����ԭ����______________��
����2����һ�������£���H2O2����H2S
��3�����Ųμӷ�Ӧ��n(H2O2)/n(H2S)�仯���������ﲻͬ����n(H2O2)/n(H2S)=4ʱ����������ķ���ʽΪ__________��
��SO2�ij�ȥ
����1��˫�������NaOH����SO2������CaOʹNaOH����
NaOH��Һ![]() Na2SO3
Na2SO3
��4��д�����̢ٵ����ӷ���ʽ��____________________________��CaO��ˮ�д�������ת����
CaO(s)+H2O (l) ![]() Ca(OH)2(s)
Ca(OH)2(s)![]() Ca2+(aq)+2OH(aq)
Ca2+(aq)+2OH(aq)
��ƽ���ƶ��ĽǶȣ��������̢�NaOH������ԭ��____________________________________��
����2���ð�ˮ��ȥSO2
��5����֪25�棬NH3��H2O��Kb=1.8��105��H2SO3��Ka1=1.3��102��Ka2=6.2��108������ˮ��Ũ��Ϊ2.0 mol��L-1����Һ�е�c(OH)=_________________mol��L1����SO2ͨ��ð�ˮ�У���c(OH)����1.0��107 mol��L1ʱ����Һ�е�c(![]() )/c(
)/c(![]() )=___________________��
)=___________________��
���𰸡� ���ͷ�Ӧ��ܣ����������� 30 �桢pH=2.0 �����ʱ��ԣ�����˾�ʧȥ���ԣ� H2SO4 2OH-+ SO2![]() SO32-+H2O SO32-��Ca2+����CaSO3������ƽ���������ƶ�����NaOH���� 6.0��10-3 0.62
SO32-+H2O SO32-��Ca2+����CaSO3������ƽ���������ƶ�����NaOH���� 6.0��10-3 0.62
����������1��������˾�����ʱ�ķ�Ӧ��������ʱ��5��105����֪����Ӧ����������������˾����������������������˷�Ӧ�Ļ�ܡ�
��2������ͼ3��֪���¶�30������ʱ���������������ͼ4��֪��pH=2.0ʱ���������������ʹ����˾����������Ϊ30�桢pH=2.0������Ӧ�¶ȹ��ߣ���˾������ʱ���ʧȥ������ɷ�Ӧ�����½���
��3�����ݻ��ϼ���������n(H2O2)/n(H2S)=4ʱ��4mol H2O2ת��8mol���ӣ���1mol H2SҲת��8mol���ӣ����ϼ۴�-2�����ߵ�+6�ۣ�������������ΪH2SO4��
��4�����̢���NaOH��SO2�ķ�Ӧ����Ӧ�����ӷ���ʽΪ2OH-+ SO2![]() SO32-+H2O������CaO��ˮ�е�ת����CaO(s)+ H2O (l)
SO32-+H2O������CaO��ˮ�е�ת����CaO(s)+ H2O (l) ![]() Ca(OH)2(s)
Ca(OH)2(s)![]() Ca2+(aq)+2OH(aq)�����̢���Na2SO3����CaO��SO32-��Ca2+����CaSO3������ƽ���������ƶ�����NaOH���ɡ�
Ca2+(aq)+2OH(aq)�����̢���Na2SO3����CaO��SO32-��Ca2+����CaSO3������ƽ���������ƶ�����NaOH���ɡ�
��5������NH3��H2O��Kb=1.8��105��֪��![]() =1.8��105������ˮ��Ũ��Ϊ2.0 mol��L-1ʱ����Һ�е�c(OH)= c(NH4+)=
=1.8��105������ˮ��Ũ��Ϊ2.0 mol��L-1ʱ����Һ�е�c(OH)= c(NH4+)=![]() =6.0��10-3 mol��L-1��
=6.0��10-3 mol��L-1��
����H2SO3��Ka2=6.2��108��֪��![]() =6.2��108������c(OH)����1.0��107 mol��L1����Һ�е�c(SO32-)/c(HSO3-)=0.62��
=6.2��108������c(OH)����1.0��107 mol��L1����Һ�е�c(SO32-)/c(HSO3-)=0.62��

����Ŀ����Դ����ϡ���Ϣһ�𱻳�Ϊ�ִ���ᷢչ������֧���������Դ�ݽߵ�Σ���������Դ�����ʺͿ�������Դ�ǽ����һ�����������Ҫ����
(1)��ѧ��Ӧ���ʺ���������������������أ����ǻ�ѧѧ�ƹ�ע�ķ���֮һ��ijͬѧΪ��̽��п�����ᷴӦ�����е����ʱ仯���� 400mL ϡ�����м���������п�ۣ�����ˮ���ռ���Ӧ�ų���������ʵ���¼����(�ۼ�ֵ):
ʱ��/min | 1 | 2 | 3 | 4 | 5 |
�������/mL(���) | 100 | 240 | 464 | 576 | 620 |
����һ��ʱ���ڷ�Ӧ�������____min(����0��1������1��2������2��3������3��4�� ����4��5��)��
����һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʵ���Ӱ��������������������Ϊ���е���____(����ĸ���)��
A.KCl ��Һ B.Ũ���� C.����ˮ D.CuSO4 ��Һ
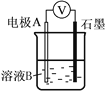
(2)��ͼΪԭ���װ��ʾ��ͼ��
���� A Ϊ����B Ϊþ�������Ϊϡ������Һ����������_______(������Ƭ������þƬ��)��
����AΪCu��B Ϊʯī�������Ϊ FeCl3 ��Һ������ʱ���ܷ�ӦΪ 2FeCl3+Cu=2FeCl2+CuCl2��д��ͭ�缫�ĵ缫��Ӧʽ��____�����õ�ط�Ӧ������ 0.1mol FeCl3�� ��ת�Ƶ��ӵ���ĿΪ _____��
����Ŀ���±���Ԫ�����ڱ���ǰ�����ڣ���ش��й����⣺�����������þ��廯ѧ����ش�
1 | �� | |||||||
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | ||||
4 | �� | �� | ||||||
��1���ܵ�ԭ�ӽṹʾ��ͼΪ_________������Ԫ�����ڱ�λ��________������Ԫ��������������ˮ����������ǿ����_________������ˮ���ﻯѧʽ��
��2���ݵ�����������ˮ����͢���������ﷴӦ�����ӷ���ʽ________________
��3���õ���ʽ��ʾԪ�آٺ͢��γɵĻ�������γɹ���________________
��4���ݵ����������ˮ����ĵ���ʽ________________
��5�������ʵ��֤��������������ǿ��________________
����Ŀ��ijС��ͬѧ����ԭ���װ��̽�����ʵ����ʡ�������ʾ��ԭ���װ���У�������Ӧ��Ļ�ԭ��Խǿ����������Ӧ���������Խǿ��ԭ��صĵ�ѹԽ��
��1��ͬѧ�������±���װ�ý���ʵ�鲢��¼��
װ�� | ��� | �缫A | ��ҺB | ���������� |
| �� | Fe | pH=2��H2SO4 | ����װ�ú�ʯī���������ɫ���ݣ���ѹ��ָ��ƫת |
�� | Cu | pH=2��H2SO4 | ����װ�ú�ʯī��������������ѹ��ָ��ƫת����¼����Ϊa |
��ͬѧ����Ϊʵ���������Ҫ���������ⸯʴ����������Ӧʽ��_____________��
�����ʵ�������ͬѧ��Ϊ�����ܷ������ⸯʴ�����ж�������_______����ͬѧ��Ϊʵ�����Ӧ����������ʴ���������ĵ缫��Ӧʽ��___________��
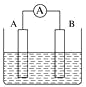
��2��ͬѧ����������װ�ò���Cu��ʯīΪ�缫����ʵ�飬̽��ʵ���ָ��ƫתԭ��Ӱ��O2���������ء�
��� | ��ҺB | ���������� |
�� | ����е�pH=2�� H2SO4 | ��Һ������ú���ǣ�����װ�ú�ѹ��ָ��ƫת����¼����Ϊb |
�� | pH=2��H2SO4 | ��ʯīһ���ͨ��O2������װ�ã���ѹ��ָ��ƫת����¼����Ϊc��ȡ���缫������Һ�м�������ŨNa2SO4��Һ��Ϻ���缫������O2ͨ�룬��ѹ��������Ϊc |
�� | pH=12��NaOH | ��ʯīһ���ͨ��O2������װ�ã���ѹ��ָ��ƫת����¼����Ϊd |
�ٱ�ͬѧ�Ƚ�ʵ����ĵ�ѹ������Ϊ��c��a��b�������ԭ����_____________��
�ڶ�ͬѧ�Ԣ��������бȽϣ���Ŀ����̽��_____________________��O2�����Ե�Ӱ�죻ʵ����м���Na2SO4��Һ��Ŀ����_____________��