题目内容
13.设NA为阿伏伽德罗常数,下列叙述正确的是( )| A. | 常温下,22g CO2含有2NA个氧原子 | |
| B. | 标准状况下,22.4L的CCl4中含有的分子数为NA | |
| C. | 1mol/L的碳酸钠溶液中含Na+离子数为2NA | |
| D. | 常温下,将含0.1NA个HCl分子的氯化氢气体溶于水配成100mL溶液,所得溶液中C(H+)为1mol/L |
分析 A、求出二氧化碳的物质的量,然后根据1mol二氧化碳中含2mol氧原子来分析;
B、标况下,四氯化碳为液态;
C、溶液体积不明确;
D、0.1NA个HCl分子即0.1mol,根据物质的量浓度c=$\frac{n}{V}$来分析.
解答 解:A、22g二氧化碳的物质的量为0.5mol,而1mol二氧化碳中含2mol氧原子,故0.5mol二氧化碳中含1mol氧原子即NA个,故A错误;
B、标况下,四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液体积不明确,故溶液中的钠离子的个数无法计算,故C错误;
D、0.1NA个HCl分子即0.1mol,溶于水后溶液体积为0.1L,故盐酸的物质的量浓度c=$\frac{n}{V}$=$\frac{0.1mol}{0.1L}$=1mol/L,由于HCl为一元强酸,则溶液中氢离子的浓度为1mol/L,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
3.将一定质量的镁.铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中正确的是( )
| A. | 当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL | |
| B. | 当金属全部溶解时收集到NO气体的体积为4.48L(标准状况下) | |
| C. | 参加反应的金属的总质量一定是9.9g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
1.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| B. | 标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 | |
| C. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3 NA | |
| D. | 常温下,1L 0.1 mol•L-1的Na2CO3溶液中含有的离子总数为0.3NA |
8.少量铁粉与100mL 0.01mol/L的稀盐酸(足量)反应,反应速率太慢.为了加快此反应速率而不改变H2的总量,可使用如下方法中的:①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L盐酸 ⑨改用100mL0.1mol/L的稀硝酸( )
| A. | ①⑥⑦ | B. | ③⑤⑧⑨ | C. | ③⑦⑧ | D. | ③⑦⑧⑨ |
10.下列叙述正确的是( )
| A. | Li在氧气中燃烧主要生成Li2O | |
| B. | 卤族元素单质X2(X:代表F、Cl、Br、I)均可以与水反应生成HX | |
| C. | 将SO2通入次氯酸钙溶液可能得到次氯酸 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
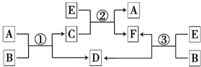 A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.
A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出. 如图,向碱式滴定管和烧杯中分别注入0.2mol•L-1Ba(OH)2溶液和0.1mol•L-1稀硫酸各50mL,并向稀硫酸中滴加几滴石蕊溶液,按如图装置连接好.
如图,向碱式滴定管和烧杯中分别注入0.2mol•L-1Ba(OH)2溶液和0.1mol•L-1稀硫酸各50mL,并向稀硫酸中滴加几滴石蕊溶液,按如图装置连接好.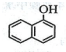 )的同分异构体,其分子中有两个官能团,能发生银镜反应,能被酸性KMnO4溶液氧化成G( C2H4O2)和芳香化合物H(C8H6O4),G和H与碳酸氢钠溶液反应均能放出CO2气体,H芳环上的一硝化产物只有一种.
)的同分异构体,其分子中有两个官能团,能发生银镜反应,能被酸性KMnO4溶液氧化成G( C2H4O2)和芳香化合物H(C8H6O4),G和H与碳酸氢钠溶液反应均能放出CO2气体,H芳环上的一硝化产物只有一种. ;
; +Cu2O↓+2H2O;
+Cu2O↓+2H2O; +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O;
+H2O; 50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: