题目内容
10.下列叙述正确的是( )| A. | Li在氧气中燃烧主要生成Li2O | |
| B. | 卤族元素单质X2(X:代表F、Cl、Br、I)均可以与水反应生成HX | |
| C. | 将SO2通入次氯酸钙溶液可能得到次氯酸 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
分析 A.Li在氧气中燃烧只生成Li2O;
B.氟气和水反应生成氧气和HF;
C.二氧化硫和次氯酸钙发生氧化还原反应生成氯化钙;
D.氨水和硫酸铜发生复分解反应.
解答 解:A.碱金属族中只有Li和氧气反应生成一种氧化物,所以Li在氧气中燃烧只生成Li2O,故A错误;
B.Cl、Br、I单质与水反应可表示为 X2+H2O=HX+HXO,氟气和水之间反应生成的是HF和氧气,反应方程式为2F2+2H2O=4HF+O2,故B正确.
C.次氯酸钙具有强氧化性,能将二氧化硫氧化生成硫酸根离子,硫酸根离子和钙离子反应生成微溶物硫酸钙,故C错误;
D.二者发生反应为2NH3.H2O+CuSO4=Cu(OH)2↓+(NH4)2SO4,故D错误;
故选B.
点评 本题考查元素化合物性质,为高频考点,明确物质性质特殊性是解本题关键,易错选项是BC,注意氟气和水反应生成氧气、二氧化硫和次氯酸钙反应生成硫酸钙,为易错点.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
13.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 常温下,22g CO2含有2NA个氧原子 | |
| B. | 标准状况下,22.4L的CCl4中含有的分子数为NA | |
| C. | 1mol/L的碳酸钠溶液中含Na+离子数为2NA | |
| D. | 常温下,将含0.1NA个HCl分子的氯化氢气体溶于水配成100mL溶液,所得溶液中C(H+)为1mol/L |
18.能鉴别SO2和CO2的试剂是( )
| A. | 品红溶液 | B. | 澄清石灰水 | C. | 紫色石蕊试液 | D. | 高锰酸钾溶液 |
5.金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料.
某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序.他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:下列有关三种金属的说法正确的是( )
某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序.他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:下列有关三种金属的说法正确的是( )
| 金属学 | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
| A. | 三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu | |
| B. | 若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg | |
| C. | 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 | |
| D. | Cu和稀盐酸不发生化学反应 |
15.将a mol的NH3与b mol的O2混合后,充入一密闭容器,在Pt存在下升温至700℃,充分反应后,冷却至室温.
(1)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
(2)当a=2.00,b=4.00,在室温下得到的产物是什么?若该产物的密度为1.44g.ml-1,则其溶质的质量分数和物质的量浓度各是多少?
(1)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
| b∕a的取值范围 | 溶质 | 溶质物质的量 |
19.下列有关说法中正确的是( )
| A. | 有单质生成的反应一定是氧化还原反应 | |
| B. | 焰色反应是元素表现出来的化学性质 | |
| C. | 由两种元素组成,原子个数比为1:1的物质一定是纯净物 | |
| D. | 能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物 |
20.下列电子式书写正确的是( )
| A. | 四氯化碳  | B. | 甲醇  | C. | 羟基  | D. | 甲基 |
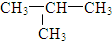 D.
D. 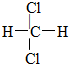 和
和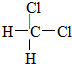 E.甲烷和庚烷
E.甲烷和庚烷