题目内容
4.下列物质属于含有共价键的离子化合物的是( )| A. | C2H2 | B. | KOH | C. | NaF | D. | C60 |
分析 活泼金属和活泼金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键.
解答 解:A.乙炔分子中只存在C-C、C-H之间的共价键,属于共价化合物,故A错误;
B.KOH中钾离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,属于离子化合物,故B正确;
C.NaF中钠离子和氟离子之间只存在离子键,为离子化合物,故C错误;
D.该物质中只存在C-C键,属于单质,故D错误;
故选B.
点评 本题考查物质和化学键关系,侧重考查基本概念,明确物质构成微粒及微粒之间作用力即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.某饱和醇1mol与O2气充分燃烧产生标况下44.8L的CO2气体,另取1mol该醇与足量的Na反应,收集到标况下22.4L的气体,则该醇为( )
| A. | CH4O | B. | CH3CH2OH | C. |  | D. | 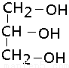 |
15.下列说法正确的是( )
| A. | 向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 | |
| B. | 欲除去Cl2中少量HCl气体,可将此混合气体通过盛饱和食盐水的洗气瓶 | |
| C. | 漂白粉的有效成分是CaCl2和Ca(ClO)2,应密闭保存 | |
| D. | 氯气有漂白性,所以氯气能使有色布条褪色 |
12.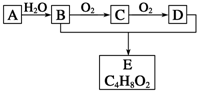 有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化学工业的发展水平.A、B、C、D、E有如图所示的关系.则下列推断正确的是( )
有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化学工业的发展水平.A、B、C、D、E有如图所示的关系.则下列推断正确的是( )
 有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化学工业的发展水平.A、B、C、D、E有如图所示的关系.则下列推断正确的是( )
有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化学工业的发展水平.A、B、C、D、E有如图所示的关系.则下列推断正确的是( )| A. | 鉴别A和甲烷可选择酸性高锰酸钾溶液 | |
| B. | B能与金属钠反应D不能 | |
| C. | 物质C和氢气反应生成乙醇,是还原反应 | |
| D. | E没有同分异构体 |
9.一定质量的Fe,Fe2O3,Fe3O4混合物与200mL 5mol•L-1盐酸恰好完反应,向反应后的溶液中加入KSCN溶液,液体不变红色,现在把相同质量的上述固体混合物在加热时与足量的氢气充分反应,可以得到固体铁的质量为( )
| A. | 28g | B. | 56g | C. | 14g | D. | 无法计算 |
13.下列有关物质的用途叙述,错误的是( )
| A. | 碳酸氢钠在医疗上可用于治疗胃酸过多 | |
| B. | 钠和钾的合金常温下是液态,可用于快中子反应堆作热交换剂 | |
| C. | 碳酸钠可用于玻璃,制皂,造纸、纺织等工业 | |
| D. | 氧化钠可用作漂白剂 |
17.下列有关NA的说法正确的是( )
| A. | 18g D2O和18g H2O中含有的质子数均为10NA | |
| B. | 2L 0.5 mol•L-1亚硫酸溶液中含有的H+离子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2mol NO和1mol O2充分反应,产物的分子数为2NA |
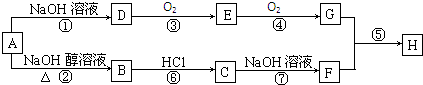
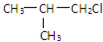 ,G的官能团名称是羧基
,G的官能团名称是羧基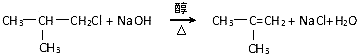 ;E与新制Cu(OH)2反应:
;E与新制Cu(OH)2反应: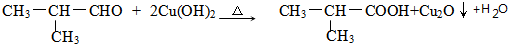 .
.