题目内容
【题目】下列说法正确的是( )
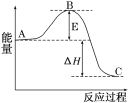
A.凡是放热反应都是自发的,凡是吸热反应都是非自发的
B.常温下反应 C(s)+CO2(g)![]() 2CO(g)不能自发进行,该反应的ΔH>0
2CO(g)不能自发进行,该反应的ΔH>0
C.自发反应的现象一定非常明显,非自发反应的熵一定减小
D.反应(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) ΔH=+74.9kJ·mol-1在高温不能自发进行
【答案】B
【解析】
G=H-ST,G<0,可自发进行。
A.放热反应H<0,S<0时,低温时自发进行,高温时非自发进行;吸热反应H>0时,高温可自发进行,A错误;
B.C(s)+CO2(g)![]() 2CO(g) S>0,常温下反应不能自发进行,G>0,该反应的ΔH>0,B正确;
2CO(g) S>0,常温下反应不能自发进行,G>0,该反应的ΔH>0,B正确;
C.自发进行的反应现象不一定非常明显,如中和反应;化学反应的方向由焓变和熵变共同决定,非自发反应的熵不一定减小,C错误;
D.反应(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) ΔH=+74.9kJ·mol-1反应中熵变、焓变皆大于0,则在高温时能自发进行,D错误;
答案为B。

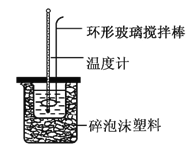
【题目】实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是_________。
(2)在操作正确的前提下,提高中和热测定准确性的关键是__________。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH=__[盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。如果用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将_______(填“偏大”、“偏小”或“不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是_________。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大