题目内容
1.1molCH2═CH-CH═CH-CH3与溴水发生加成反应最多需要多少溴水( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
分析 CH2═CH-CH═CH-CH3的官能团为碳碳双键,而1mol碳碳双键能和1molBr2发生加成反应,据此分析.
解答 解:CH2═CH-CH═CH-CH3的官能团为碳碳双键,是一种二烯烃,1molCH2═CH-CH═CH-CH3中含2mol碳碳双键,而1mol碳碳双键能和1molBr2发生加成反应,故1molCH2═CH-CH═CH-CH3中含2mol碳碳双键,则最多能消耗2mol溴水,故选B.
点评 本题考查了烯烃与溴的加成反应,应注意的是CH2═CH-CH═CH-CH3是一种二烯烃,内含2个碳碳双键.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
11.下列说法不正确的是( )
| A. | 某微粒空间构型为三角锥形,则该微粒一定是极性分子 | |
| B. | 某微粒空间构型为V形,则中心原子一定有孤电子对 | |
| C. | NH4+中N-H键能、键长和键角均相同 | |
| D. | SiF4和SO${\;}_{3}^{2-}$的中心原子均为sp3杂化,其立体构型都是正四面体 |
12.下列有关电解质溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 在0.1mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol•L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
9.下列物质中,有共价键的单质是( )
| A. | N2 | B. | CH4 | C. | NaCl | D. | MgCl2 |
6.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 11.2 LNH3中所含的质子数为5NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA个 | |
| C. | 2.4g金属镁变为Mg2+时失去的电子数为0.1 NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为 NA 个 |
13.有A、B、C、D四种金属,分别把它们加入到稀盐酸中,A、B、D反应后有气体放出,C无明显现象,再把A、D加入B盐溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序是为( )
| A. | A>B>D>C | B. | B>D>A>C | C. | D>A>B>C | D. | D>B>A>C |
4.X、Y、Z、W、M为原子序数依次增大的短周期主族元素.已知①元素对应的原子半径大小为:X<Z<Y<M<W ②原子的最外层电子数:X=W,X+Y=Z=2M ③Y元素的主要化合价:最高正价+最低负价=2,下列说法不正确的是( )
| A. | X、Z两种元素可形成X2Z和X2Z2两种常见共价化合物 | |
| B. | M与Z形成的化合物的分子式为M2Z3 | |
| C. | 工业上可用电解熔融的W的氯化物的方法制取W的单质 | |
| D. | Z元素对应的单质与W元素对应的单质在不同条件下反应产物可能不同 |
 ,CO2
,CO2 .
.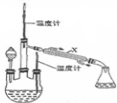 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl