题目内容
6.NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 11.2 LNH3中所含的质子数为5NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA个 | |
| C. | 2.4g金属镁变为Mg2+时失去的电子数为0.1 NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为 NA 个 |
分析 A、氨气所处的状态不明确;
B、求出Na2CO3的物质的量,然后根据1molNa2CO3中含2mol钠离子来分析;
C、求出镁的物质的量,然后根据1mol镁变为镁离子时失去2mol电子来分析;
D、溶液体积不明确.
解答 解:A、氨气所处的状态不明确,不一定是标况,故物质的量不一定是0.5mol,则含有的质子的物质的量不一定为5mol,故个数不一定是5NA,故A错误;
B、1.06gNa2CO3的物质的量n=$\frac{1.06g}{106g/mol}$=0.01mol,而1molNa2CO3中含2mol钠离子,故0.01mol碳酸钠中含0.02mol钠离子,即0.02NA个,故B正确;
C、2.4g镁的物质的量为0.1mol,而1mol镁变为镁离子时失去2mol电子,故0.1mol镁失去0.2mol电子,即0.2NA个,故C错误;
D、溶液体积不明确,故氯离子的个数无法求算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
14.下列有机物分子中,相邻的五个原子可以构成一个正四面体的是( )
| A. | CHCl3 | B. | CH(CH3) 3 | C. | CCl4 | D. | CH3CH3 |
1.1molCH2═CH-CH═CH-CH3与溴水发生加成反应最多需要多少溴水( )
| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
18.NA表示阿伏加德罗常数,下列说法错误的是( )
| A. | 1molNH3中含有6.02×1024个电子 | |
| B. | 1mol水中含有2mol氢和1mol氧 | |
| C. | 1molOH-中含有8mol中子 | |
| D. | 2.3g钠由原子变成离子时,失去的电子数为0.1NA |
 在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)?2HI(g)△H<0,反应中各物质的浓度随时间变化情况如图1:
在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)?2HI(g)△H<0,反应中各物质的浓度随时间变化情况如图1:

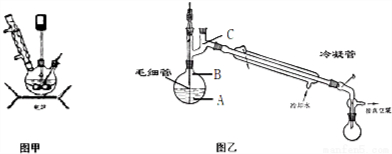 水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途.用尿素法制水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:CO (NH2)2+NaClO+2NaOH→H2N-NH2•H2O+NaCl+Na2CO3.
水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途.用尿素法制水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:CO (NH2)2+NaClO+2NaOH→H2N-NH2•H2O+NaCl+Na2CO3.