题目内容
【题目】在同温同压下,下列各组热化学方程式中Q2 > Q1的是( )
A. 2H2(g)+O2(g)=2H2O(l) ΔH== -Q1 2H2(g)+O2(g)=2H2O(g) ΔH== - Q2
B. S(g)+O2(g)=SO2(g) ΔH== - Q1 S(s)+O2(g)=SO2(g) ΔH== - Q2
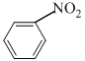
C. C(s)+![]() O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
O2(g)=CO(g) ΔH== - Q1 C(s)+O2(g)=CO2(g) ΔH== - Q2
D. H2(g)+Cl2(g)=2HCl(g) ΔH== - Q1 ![]() H2(g)+
H2(g)+![]() Cl2(g)= HCl(g) ΔH== - Q2
Cl2(g)= HCl(g) ΔH== - Q2
【答案】C
【解析】
选项中的反应都为放热反应,由热化学方程式可知Q越大,放出的热量越多,物质反应的越彻底,参加反应的物质的量越多,放出的热量越多,物质的聚集状态不同,Q不同,以此解答该题。
A.H2O(气)→H2O(液)为放热过程,则Q2<Q1,选项A错误;
B.S(固)→S(气)为吸热过程,则Q2<Q1,选项B错误;
C.因CO(气)→CO2(气)为放热过程,后者反应比较彻底,放出的热量更多,则Q2>Q1,选项C正确;
D.参加反应的物质越多,放出的热量越多,则Q2<Q1,选项D错误;
答案选C。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示。根据该表,回答下列问题:
化学式 | HF | CH3COOH | H2SO3 | H2CO3 | H2S |
电离平衡 常数(Ka) | 4.0×10-4 | 1.8×10-5 | K1=1.54×10-2 K2=1.02×10-7 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
(1)同浓度的F-、CO32-、CH3COO-、HS-结合H+的能力最强的为__________
(2)溶液中不可能大量共存的离子组是__________
a.HS-、SO32- b.HF、CH3COO- c.HS-、HCO3- d. HSO3-、HCO3-
(3)Na2CO3溶液通入过量H2S的离子方程式是:_____。
(4)OH-浓度相同的等体积的两份溶液HCl(A)和 CH3COOH(E),分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_______(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
(5)向 0.l molL-1 CH3COOH溶液中滴加 NaOH 溶液至c(CH3COOH) : c(CH3COO-) =2 : 36,此时溶液pH = __________。