题目内容
【题目】已知某可逆反应:mA(g) + nB(g)![]() pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g) H= Q kJ·mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
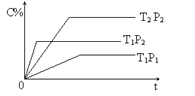
A. T1<T2 P1>P2 m+n<P Q<0B. T1>T2 P1<P2 m+n>P Q>0
C. T1<T2 P1<P2 m+n<P Q>0D. T1>T2 P1<P2 m+n>P Q<0
【答案】D
【解析】
本题主要考查化学平衡相关图像。根据先拐先平原则判断T1与T2、P1与P2相对大小,再根据勒夏特列原理判断该反应的系数关系以及焓变的正负。
根据先拐先平可知,T1>T2,P1<P2,根据定一议二可知,相同压强下,升高温度,C的百分含量降低,即升高温度,反应逆向移动,故该反应正向的H<0;相同温度下,增大压强,C的百分含量升高,即增大压强,反应正向移动,故m+n>P,故答案为D。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系不正确的是 ( )
选项 | 现象或事实 | 解释 |
A | Na2O2常用于潜水艇或呼吸面具的供氧剂 | Na2O2与H2O、CO2反应产生O2 |
B | 常用铝箔做包装材料 | 金属铝有好的延展性 |
C | FeCl3溶液可用于刻制印刷铜电路板 | FeCl3可与Cu发生反应 |
D | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | 烧菜时铁锅被染色 |
A.AB.BC.CD.D
【题目】用活性炭还原法处理氮氧化物,有关反应为:C(s)+ 2NO(g)![]() N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
时间min/ 浓度mol·L-1 | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
(1) 10 min~20 min的时间段内,以CO2表示的反应速率为____;
(2)计算出该反应的平衡常数的值K=________;
(3) 下列各项能作为判断该反应达到平衡状态的是____ (填序号字母);
A.容器内压强保持不变 B.2v正(NO)= v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是_____________;
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率__________ (填“增大