题目内容
【题目】某探究小组设计如右图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:


(1)仪器A中发生反应的化学方程式是______;装置B中的试剂是_______。
(2)若撤去装置C,可能导致装置D中副产物_____(填化学式)的量增加;装置D可采用 加热的方法以控制反应温度在70℃左右。
(3)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH。你认为此方案是否可行,为什么?_______________。
(4)装置E中可能发生的无机反应的离子方程式有_________________。
(5)测定产品纯度:称取产品0.30 g配成待测溶液,加入0.1000 mol·L-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 mo1·L-1Na2S2O3溶液滴定至终点。进行平行实验后,测得消耗Na2S2O3溶液20.00 mL。则产品的纯度为_________。(CCl3CHO的相对分子质量为147.5)滴定的反应原理:CCl3CHO+OH-==CHCl3+HCOO-、HCOO-+I2==H++2I-+CO2↑ 、I2+2S2O32-==2I-+S4O62-
(6)已知:常温下Ka(CCl3COOH)=1.0×10-1mol·L-1,Ka (CH3COOH)= 1.7×10-5mol·L-1,请设计实验证明三氯乙酸、乙酸的酸性强弱。
【答案】(1)4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O 饱和食盐水
MnCl2+Cl2↑+2H2O 饱和食盐水
(2)CCl3COOH 水浴
(3)不行,三氯乙酸可溶于乙醇
(4)Cl2 + 2OH-==Cl- + ClO- + H2O H+ + OH-==H2O
(5)88.5%分别测定0.1mol·L—1两种酸溶液的pH,三氯乙酸的pH较小,证明三氯乙酸的酸性强于乙酸
【解析】
试题分析:本题考查三氯乙醛(CCl3CHO)的实验制备。分析题给装置知A装置利用二氧化锰与浓盐酸制备氯气,B装置用饱和食盐水除去HCl,C装置盛放浓硫酸干燥氯气,D中反应制备CCl3CHO,E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气,据此解答。
(1)仪器A中二氧化锰与浓盐酸在加热条件下反应生成二氯化锰、氯气与水,化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)C装置用浓硫酸除去氯气中的水蒸气,减少副反应发生,撤去C装置,氯气中混有水蒸气,增大副反应CCl3CHO+HClO→CCl3COOH+HCl,导致装置D中副产物CCl3COOH 增多;根据表中各物质的沸点数据判断为防止原料和产品的挥发,应采取水浴加热,受热均匀,偏于控制温度。
(3)CCl3COOH易溶于乙醇与CCl3CHO,应采取蒸馏方法进行分离,答案为:不可行,CCl3COOH溶于乙醇与CCl3CHO。
(4)E装置盛放氢氧化钠溶液,吸收尾气中氯气、HCl防止污染空气,反应离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O、H++OH﹣=H2O。
(5)根据消耗的Na2S2O3计算剩余I2的物质的量0.02000molL﹣1×0.02L=2×10﹣4mol,与HCOO﹣反应的I2的物质的量为0.1000molL﹣1×0.02L﹣2×10﹣4mol=1.8×10﹣3mol,由CCl3CHO~HCOO﹣~I2可知,CCl3CHO的物质的量为1.8×10﹣3mol,则产品的纯度为(1.8×10﹣3mol ×147.5g/mol)/0.3g×100%=88.5%。
(6)酸性越强,电离程度越大,浓度相同时溶液pH越小,故实验方案为分别测定0.1mol·L—1两种酸溶液的pH,三氯乙酸的pH较小,证明三氯乙酸的酸性强于乙酸。

 黄冈小状元同步计算天天练系列答案
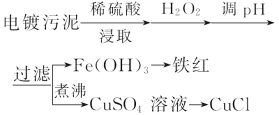
黄冈小状元同步计算天天练系列答案【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是 。调pH步骤中加入的试剂最好是 (填化学式)。实验室进行过滤操作所用到的玻璃仪器有 、 、 。
(2)煮沸CuSO4溶液的原因是 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式 。
(3)Fe3+发生水解反应Fe3++3H2O![]() Fe(OH)3+3H+,该反应的平衡常数表达式为 。
Fe(OH)3+3H+,该反应的平衡常数表达式为 。
(4)称取所制备的CuCl样品0.250 0 g置于一定量的0.5 mol·L-1FeCl3溶液中,待样品完全溶解后,加水20 mL,用0.100 0 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00 mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数 。







