题目内容
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是 。调pH步骤中加入的试剂最好是 (填化学式)。实验室进行过滤操作所用到的玻璃仪器有 、 、 。
(2)煮沸CuSO4溶液的原因是 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式 。
(3)Fe3+发生水解反应Fe3++3H2O![]() Fe(OH)3+3H+,该反应的平衡常数表达式为 。
Fe(OH)3+3H+,该反应的平衡常数表达式为 。
(4)称取所制备的CuCl样品0.250 0 g置于一定量的0.5 mol·L-1FeCl3溶液中,待样品完全溶解后,加水20 mL,用0.100 0 mol·L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00 mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数 。
【答案】(1)将Fe2+氧化成Fe3+,便于调整pH使其与Cu2+分离 CuO[或Cu(OH)2等]
漏斗、烧杯、玻璃棒
(2)除净溶液中的H2O2,避免影响下一步CuCl的生成
2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+2Na2SO4+H2SO4
(3)K=![]() ,
,
(4)99.50%
【解析】
试题分析:(1)电镀污泥中含有铜、铁等金属化合物,酸浸后主要是溶解铜、铁等金属化合物,双氧水有强氧化性,能氧化具有还原性的物质,Fe2+ 具有还原性,酸浸后加入H2O2,Fe2+ 能被双氧水氧化为铁离子,便于调整pH值与Cu2+ 分离;调整pH步骤中加入的试剂最好是加入某种物质除去溶液中的酸且不引进新的杂质,所以要加入CuO或Cu(OH)2 或CuCO3;要使三价铁离子和铜离子分离,过滤操作用到的仪器有铁架台、漏斗、烧杯、玻璃棒等;其中属于玻璃仪器有:漏斗、烧杯、玻璃棒;
(2)过氧化氢性质比较稳定,若加热到153℃便猛烈的分解为水和氧气,将溶液中过量的H2 O2 除去可加热至沸避免影响下一步CuCl的生成;因为CuSO4 中+2价的铜能把Na2SO3 中+4价的硫氧化成+6价的硫,向CuSO4 溶液中加入一定量的NaCl、Na2SO3 时生成白色的CuCl沉淀,反应的化学方程式是2CuSO4+2NaCl+ Na2SO3+H2O=2CuCl↓+2Na2SO4+H2SO4;
(3)化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与个反应物浓度的幂指数乘积的比。因此该水解反应飞平衡常数K=![]() 。
。
(4)由方程式可得关系式为CuCl~Fe2+~Ce4+。n(Ce4+)=n(CuCl)=c·V=0.1000mol/L ×0.025L=2.5×10-3mol,所以m=n·M=2.5×10-3mol×99.5=0.24875g,所以该CuCl样品的质量分数为:![]() ×100%=99.50%。
×100%=99.50%。

【题目】A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A | ||||||
B | C[ | D | ||||
E | F | G | H | |||
请回答下列问题:
(1)写出E元素在周期表中的位置 。
(2)B与D可形成三原子分子X,X的电子式为 。
(3)E、F、H所形成的简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)G的最高价氧化物与B的单质在高温下能发生置换反应,其化学反应方程式为:
。
(5)由A、C、D三种元素组成的强电解质Z溶于水时能促进水的电离,测得Z的水溶液pH<7,其原因是 (用离子方程式来表示)。
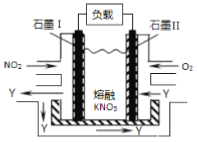
(6)盐Y由B、D、E组成。以熔融盐Y为电解质构成的燃料电池如图所示。
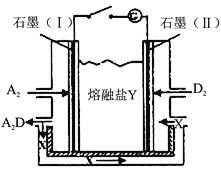
写出石墨(I)电极上发生的电极反应式 。
(7)用熔融盐Y的燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为 。