题目内容
【题目】以下实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
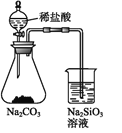
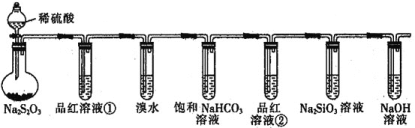
A | 证明非金属性强弱:Cl>C>Si |
|
B | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
C | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
D | 证明相同温度下: Ksp(Ag2S)<Ksp(AgCl) | 向2 mL 0.1 mol·L-1硝酸银溶液中加入1 mL 0.1 mol·L-1 NaCl溶液,出现白色沉淀,再加入 几滴0.1 mol·L-1 Na2S溶液,有黑色沉淀生成 |
A.AB.BC.CD.D
【答案】B
【解析】
A.稀盐酸属于无氧酸,不是最高价氧化物对应的酸,所以不能根据2HCl+Na2CO3=2NaCl+H2O+CO2↑,证明非金属性Cl>C,另外盐酸挥发,无洗气装置,A错误;
B.氯水与NaBr和KI反应分别生成Br2、I2,两者都易溶于CCl4,分别在CCl4层中显橙红色、紫红色,B正确;
C.NaHCO3受热易分解,而Na2CO3受热不易分解,不能达到除杂目的,C错误;
D.硝酸银与氯化钠反应,硝酸银过量,硫化钠与溶液中的银离子直接反应,无法证明哪种沉淀的溶度积更小,D错误;
故选B。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】经测定乙醇的分子式是![]() ,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
Ⅰ. 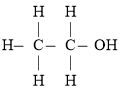 Ⅱ.
Ⅱ. 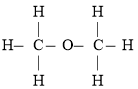
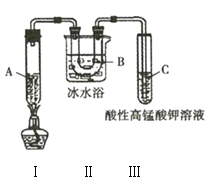
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生利用如图所示装置进行实验确定乙醇分子的结构。图中量气装置由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200mL),供量气用;乙管可.上下移动,以调节液面高低。
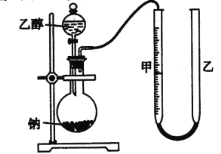
(1)学生甲得到一组实验数据:
乙醇的物质的量 | 氢气的体积(标准状况下) |
0.01mol | 0.112L |
根据以,上数据推断,乙醇的结构应为_______(填“I”或“Ⅱ”),原因是______。
(2)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性外,在读取反应前后甲管中液面读数的过程中,应注意_______(填序号)。
a 视线与凹液面最低处相平
b 等待片刻,待乙管中液面不再上升时,立刻读数
c 读数时应上下移动乙管,使甲、乙两管液面相平
d 读数时不一定使甲、乙两管液面相平
(3)学生丙不想通过称取乙醇的质量来确定乙醇的物质的量,那么他还需要知道的数据是________。
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )
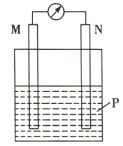
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 锌 | 稀硫酸 |
C | 银 | 锌 | AgNO3溶液 |
D | 铜 | 铁 |
|
A.AB.BC.CD.D